
Le RDM est bien reporté au 26 mai 2021 !
Tout est allé plus rapidement qu'on ne l'avait imaginé. Le report d'un an du règlement (UE) 2017/745 proposé par la Commission européenne le 3 avril a été adopté par le Conseil et le Parlement. On [...]

Tout est allé plus rapidement qu'on ne l'avait imaginé. Le report d'un an du règlement (UE) 2017/745 proposé par la Commission européenne le 3 avril a été adopté par le Conseil et le Parlement. On [...]

Le Cetim vient de réaliser, en collaboration avec le Snitem et une dizaine d'industriels, un nouveau guide intitulé "Maîtrise de la sous-traitance dans le secteur des dispositifs médicaux". Cet ouvrage a pour but d'aider les [...]
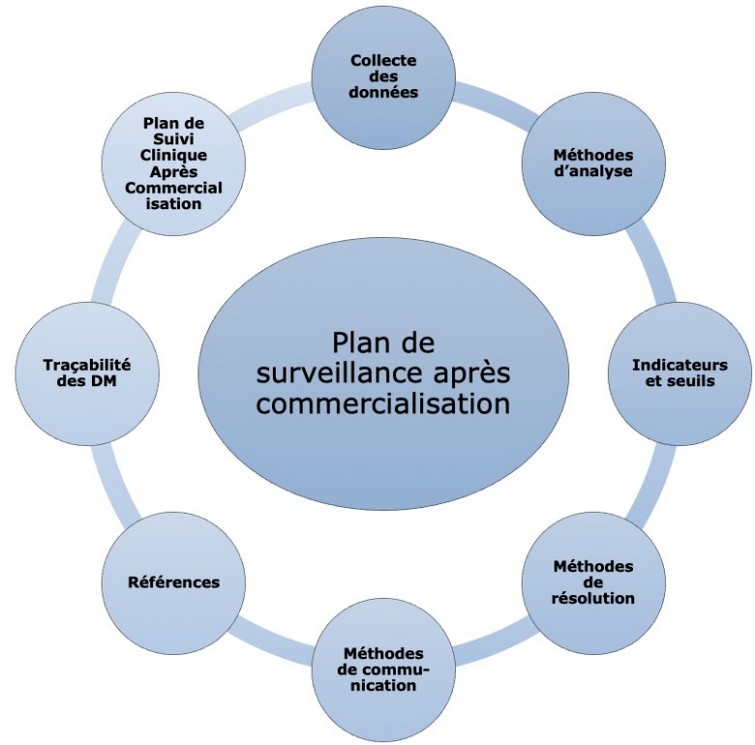
Des élèves de l'Université de Technologie de Compiègne (UTC) ont développé, dans le cadre d'un mémoire de Master, un guide composé de deux outils, disponibles gratuitement en ligne. Sa vocation est d'aider les fabricants de [...]

Le MDCG (Medical Device Coordination Group) vient de publier des directives sur les mesures extraordinaires liées aux audits des organismes notifiés en période de restrictions dues au COVID-19. Ces directives sont valables jusqu'à la fin [...]

Dans le cadre de la validation des procédés de nettoyage selon la norme ISO 19227, le laboratoire Albhades recommande de recourir à des méthodes spécifiques d'analyse pour la recherche de contaminants inorganiques. Cet article nous [...]

Alors que l'association Medtech Europe appelait, le 23 mars dernier, à reporter la mise en œuvre du RDM, la Commission européenne a annoncé, deux jours après, travailler sur une proposition de report d'un an, qui [...]

La liste des organismes notifiés selon le règlement (UE) 2017/745 (RDM) vient d'être mise à jour sur le site NANDO de la Commission européenne, avec l'ajout de CE Certiso Orvos, basé en Hongrie. Les codes produits [...]

Même si la mise en application obligatoire du RDM a été repoussée d’un an, il est recommandé aux fabricants d’actualiser dès aujourd’hui leurs informations sur le système d’identification unique des dispositifs médicaux. La société Foba [...]

A deux mois de l’entrée en vigueur de la nouvelle réglementation sur les dispositifs médicaux (RDM), le Snitem fait un point complet sur les changements qu’elle induit, avec la publication d’un document de synthèse au [...]

Swiss Medtech l'a annoncé récemment : l'accord de reconnaissance mutuelle entre la Suisse et l'UE ne couvrira très probablement plus les DM sous le règlement UE 2007/745 ni ceux certifiés selon la directive 93/42/CE. Une [...]

L’utilisabilité est une caractéristique importante d’un DM qu'il est essentiel d'intégrer très en amont du projet d'interface utilisateur. UseConcept nous explique ici combien il est intéressant de recourir au maquettage de cette interface, tant pour [...]
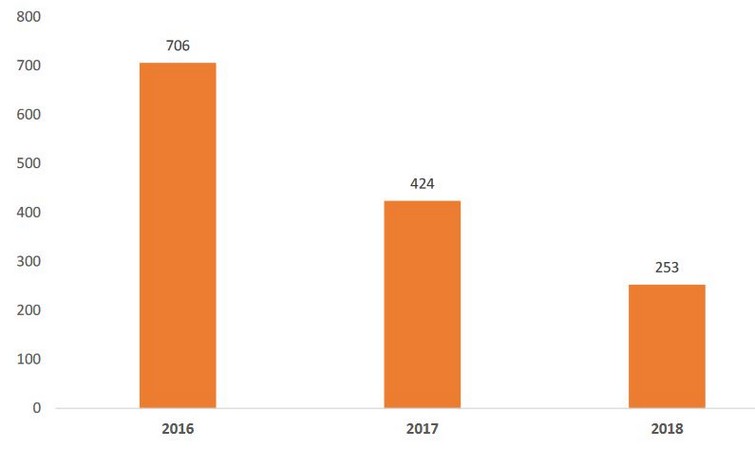
Le 27 février prochain, la HAS organise un webinaire pour expliquer comment préparer et déposer son dossier d'évaluation sur la plate-forme dématérialisée sésame, mise en place en avril 2019. Les spécificités des DM connectés et [...]

La liste des organismes notifiés selon le règlement (UE) 2017/745 (RDM) a été mise à jour le 6 février dernier sur le site NANDO de la Commission européenne, avec l'ajout de DNV GL Presafe AS, [...]

La liste des organismes notifiés selon le règlement (UE) 2017/745 (RDM) vient d'être mise à jour sur le site NANDO de la Commission européenne, avec l'ajout de NSAI (National Standards Authority of Ireland), basé en [...]

Malgré le report à mai 2022 de la disponibilité de la base de données Eudamed, les fabricants de DM ne doivent pas tarder à établir une stratégie de publication des données UDI. Cela exige de [...]

Le RDM devient obligatoire le 26 mai prochain. A compter de cette date, tout nouveau DM devra faire l'objet d'une demande de marquage CE en vertu de ce nouveau règlement. Mais qu'en sera-t-il des "legacy [...]
Les exigences des nouveaux règlements européens relatifs aux dispositifs médicaux (RDM et RDIV) n’épargnent pas les sociétés pharmaceutiques produisant des DM combinés ou des diagnostics compagnons. Cet article du cabinet de conseil Maetrics vise à [...]

Dans un communiqué publié par MedTech Europe à la fin du mois dernier, l'association européenne de l'industrie des technologies médicales exprime son inquiétude concernant la mise en oeuvre du nouveau cadre réglementaire, tout particulièrement en [...]

La publication récente du 2ème corrigendum au règlement (UE 2017/745) a incité le cabinet White-Tillet à une réflexion globale sur la nouvelle réglementation bientôt applicable aux dispositifs médicaux (DM). La Commission européenne a publié le 25 [...]
Depuis la publication, dans le numéro de Septembre/Octobre 2019 de DeviceMed, de l'article de Covartim sur la réglementation européenne des dispositifs médicaux de type logiciel, la situation a nettement évolué et des précisions ont été apportées [...]

Dans cet article, nous avons demandé à deux experts en droit des sciences de la vie d'exposer la marche à suivre par les fabricants de dispositifs médicaux en cas de défaillance d'un organisme notifié (ON) [...]

Afin de constituer 12 groupes d'experts dans le cadre de la nouvelle réglementation sur les DM et DMDIV, la Commission européenne a lancé un appel à manifestation d'intérêt avec une échéance au 10 novembre prochain. Le [...]
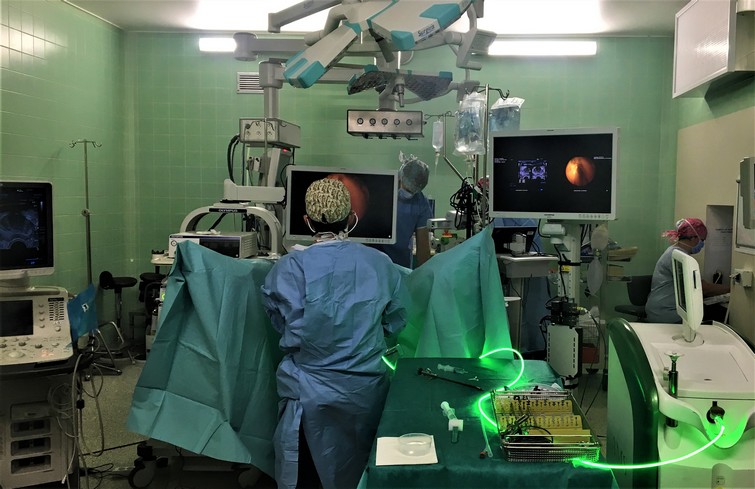
Fruit de 3 ans et demi de recherches, le standard DICOM-RTV (pour Real-Time Video) est un aboutissement important pour les équipes de l’institut de recherche technologique (IRT) b<>com et le DICOM Standards Committee, ainsi qu’une [...]
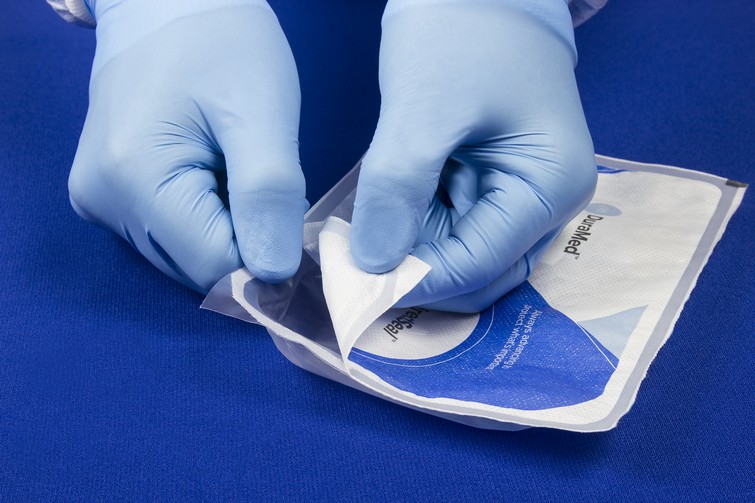
Norme clé pour la maîtrise du conditionnement des dispositifs médicaux stériles, l’ISO 11607-1 a fait l’objet d’une révision en 2019. Le cabinet de conseil Aexiqual explique ici les principales évolutions de ce texte. Jean-François Biron (source [...]

Invitée du Snitem à la dernière Journée start-up innovantes du dispositif médical, Clémentine Liard est venue partager son expérience en tant que responsable Qualité/Affaires réglementaires chez Robocath. Un témoignage riche de bonnes pratiques à suivre [...]

En cours de finalisation, le projet de norme XP S99-223 concerne la gestion du rapport bénéfice/risque des dispositifs médicaux. Porté par la commission de normalisation française Afnor/S95B, il a été initié en réponse aux exigences [...]

Spécialiste du secteur de la santé, le cabinet de conseil international Maetrics alerte, dans cet article, les fabricants de dispositifs médicaux de classe I en examinant quatre défis clés que représente pour eux le règlement [...]

Après BSI en janvier, c'est au tour de TÜV Süd d'être notifié par la Commission européenne au titre du règlement (UE) 2017/745. L'occasion pour nous de faire un nouveau point sur l'état d'avancement quantitatif des [...]

Par ses explications et ses conseils pratiques, le dernier livre blanc de Maetrics intéressera les fabricants de DM de classe I confrontés à leur obligation de mise en conformité avec le règlement (UE) 2017/745 à [...]
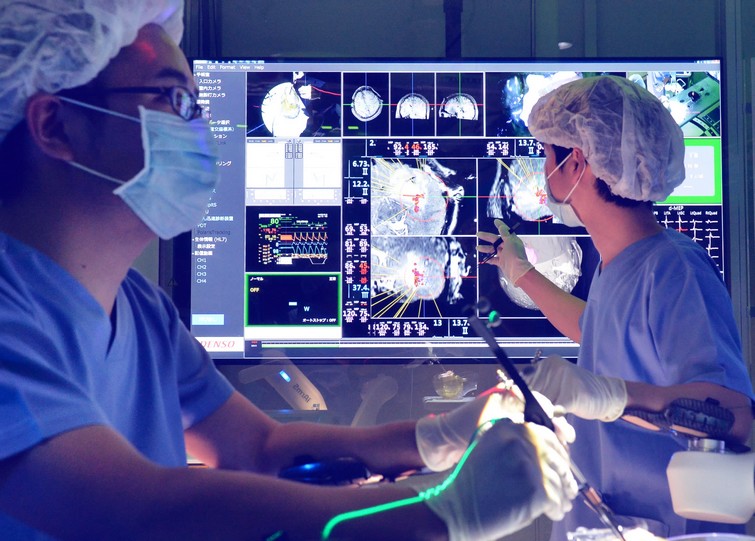
Pionnier du conseil en ergonomie, Human Design Group accompagne les fabricants de DM pour la mise en œuvre de la norme IEC 62366:2015 mais aussi, plus largement, sur le développement de produits simples, sûrs, efficaces et [...]

La surveillance accrue des organismes notifiés les amène eux-mêmes à redoubler de vigilance lors de l'évaluation de la conformité des dispositifs médicaux. La conduite d'audits inopinés chez les fabricants fait partie de leurs obligations. Les [...]

Alors que le premier organisme notifié (ON), BSI au Royaume-Uni, vient d’être désigné par la Commission européenne au titre du règlement (UE) 2017/745, l’inquiétude demeure parmi les ON qui doutent fort que tous les fabricants [...]
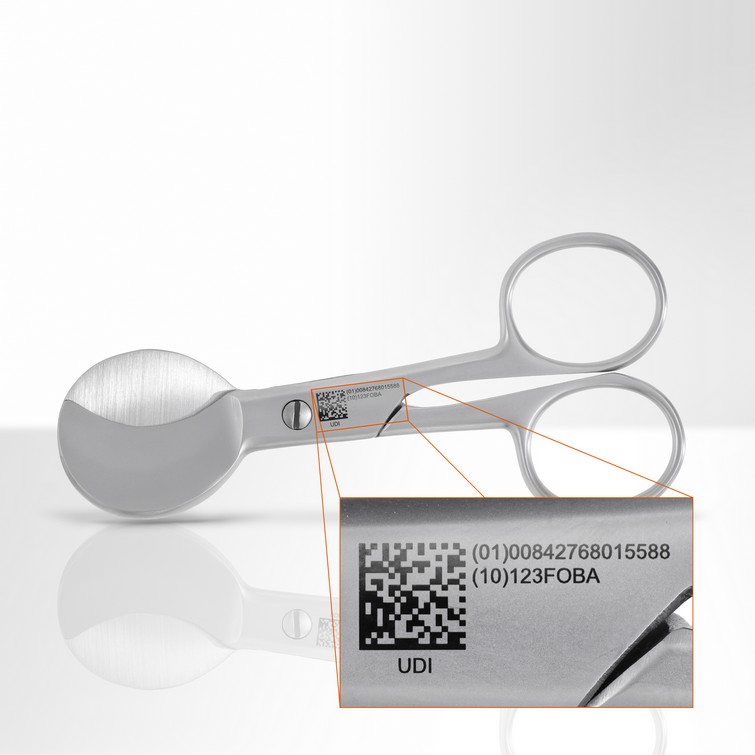
Comment les fabricants de DM doivent-il se préparer à l'UDI ? C'est la question à laquelle trois experts des entreprises Oticon, Johnson & Johnson et Convatec ont répondu lors d'une table ronde organisée par Pharma [...]

Spécialisée dans l'accompagnement réglementaire de fabricants de dispositifs médicaux, la société nexialist est de plus en plus souvent saisie pour des missions de sauvetage d'urgence du marquage CE de ses clients. Des situations dont ces [...]

Les fabricants de dispositifs médicaux sont invités à participer à l'European UDI Forum 2019 qui se déroulera à Bruxelles les 24 et 25 avril prochains, pour tout savoir des mesures à prendre en matière de [...]

Les nouveaux Règlements DM et DMDIV entreront respectivement en application en 2020 et 2022. Lors de la Rentrée du DM 2018, Corinne Delorme a dressé un bilan de l’avancement des travaux d’interprétation et des mesures [...]

Co-édité par le Cetim et le Snitem, ce guide pratique revient, étape par étape, sur le processus à mettre en œuvre pour assurer l’aptitude à l’utilisation des DM dans le respect de la norme EN [...]

Qualitiso a publié sur son blog deux articles intéressants sur l'aptitude à l'utilisation : l'un sur le nombre d'utilisateurs à impliquer dans les évaluations sommatives, l'autre sur les causes classiques d'erreurs d'utilisation des DM, avec [...]

Entreprise de conseil spécialisée dans les exigences du secteur des DM, Qualitiso se distingue par la mise à disposition d’articles et de ressources en lignes bien utiles pour les fabricants, comme c'est le cas de [...]

La cybersécurité des DM est devenue une préoccupation majeure des fabricants et des organismes de santé, avec pour enjeux principaux la protection des patients et le respect de la confidentialité des données de santé. Quels [...]

Face à l'ampleur des évolutions normatives et réglementaires et en réponse aux modes de travail actuels, DM Experts a décidé de lancer son "Académie" : une formation à distance dont la première session concerne le règlement [...]

Le nouveau livre blanc de Maetrics souligne les changements de conformité qui s’appliqueront aux rapports d'évaluation cliniques au regard de la nouvelle règlementation européenne des dispositifs médicaux, et comment les interpréter. Cabinet de conseil en matière [...]

Le Snitem a mis un outil web sécurisé, unique en son genre, à la disposition de ses adhérents, pour les aider à se mettre en conformité avec le nouveaux règlement européen sur les dispositifs médicaux. [...]

Les fabricants d'implants à base de CrCo sont aujourd'hui tributaires d'une décision imminente du comité REACH consistant à reclassifier le cobalt métallique en substance potentiellement cancérigène. Une situation qui pourrait bien mettre cette profession en [...]
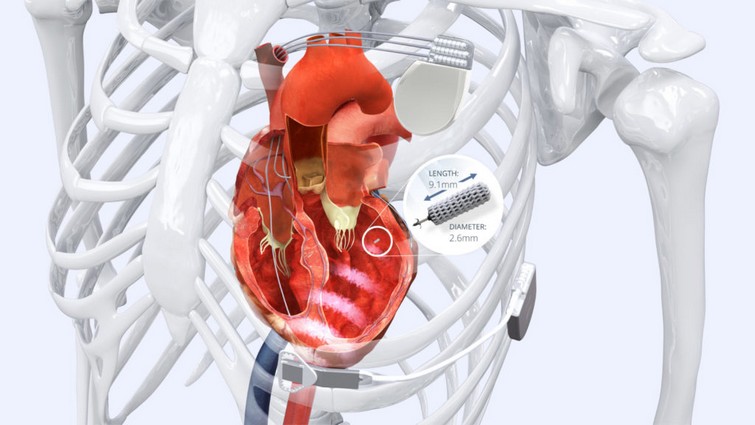
Au cours de l'été dernier, le collège de la HAS a rendu 3 avis scientifiques favorables à l’attribution du Forfait Innovation, dont un concerne pour la première fois un DM implantable en cardiologie : le [...]
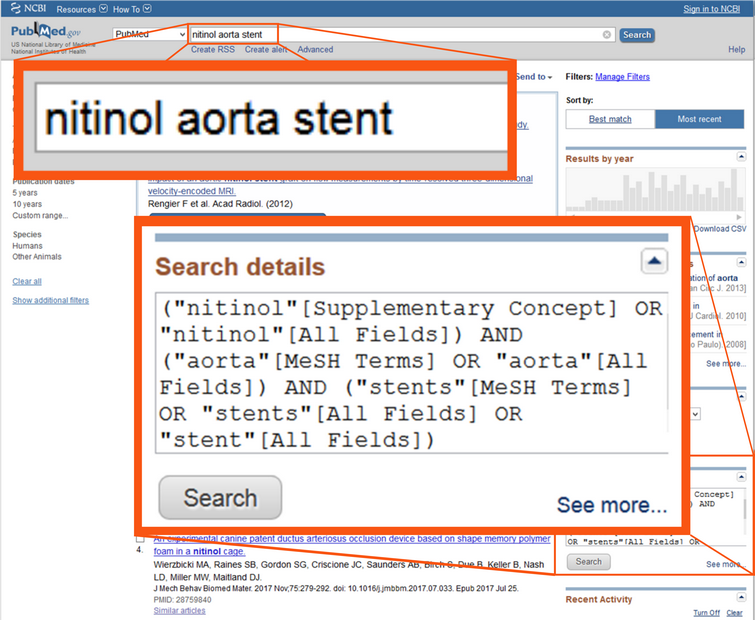
Les recherches bibliographiques, à des fins d'évaluation clinique notamment, recèlent certains pièges qu'une application spécialisée permet d'éviter. Patrick Raugel de Meddeva nous donne l'exemple du changement récent d'une expression booléenne dans la base de données [...]

La norme ISO 14607 définit de nouvelles méthodes d'essai et critères d’acceptation concernant les implants mammaires. Le LNE devrait être le premier laboratoire reconnu compétent en la matière. En France, 340000 femmes sont porteuses d’implants mammaires [...]

Avec son application ECG embarquée dans l’Apple Watch Series 4, le géant de l'électronique entre de plain-pied sur le marché du dispositif médical qui n'était pour lui qu'une niche jusqu'ici. La révolution est au rendez-vous, [...]

De la désignation des organismes notifiés dépendent les démarches de mise en conformité des DM avec les nouveaux règlements européens. Nous avons interrogé Françoise Schlemmer, directrice de Team-NB, pour savoir où nous en sommes de [...]

La 7ème Rencontre AFCROs & DM sera l'occasion de faire le point sur l'actualité réglementaire de l'évaluation clinique du dispositif médical, avec la participation du CEPS, du CNRIPH, de la CNEDIMTS, de la CNIL, du [...]