
DeviceMed Septembre/Octobre 2020
Publié le 02 septembre 2020 [...] R • Matériau PPSU approuvé par la FDA Au sommaire de notre prochain Evénements à venir numéro Medi'Nov Connection Câble BioCompatic [...]

Publié le 02 septembre 2020 [...] R • Matériau PPSU approuvé par la FDA Au sommaire de notre prochain Evénements à venir numéro Medi'Nov Connection Câble BioCompatic [...]

Publié le 21 juillet 2020 [...] artenaires du secteur de la construction mécanique pour développer le moniteur de contrôle maXYmos TL ML, dans le strict respect des directives de la FDA et du règlement européen sur les dispositifs médicaux (RDM). Un moniteur de contrôle avec des fonctionnalités conformes à la

Publié le 01 juillet 2020 [...] RDM d'un produit ou une ap- 2.0 se distingue par une nou- Le deuxième produit, cuments de conformité et des plication FDA 510K. eg velle interface intuitive, des Regislate, dédié à la gestion délais. www.arazygroup.com 6 [...]

Publié le 23 juin 2020 [...] cer la sécurité du patient mais aussi d‘éviter les contrefaçons. Unique Device Identification (UDI) Alors que le système UDI élaboré par la FDA est déjà en application aux Etats-Unis et rend obligatoires l’enregistrement et l’identification des dispositifs médicaux, l’Europe s’apprête à impos [...]

Publié le 09 juin 2020 [...] oncerne les projets monopartenaires ou collaboratifs, privés ou publics pouvant porter sur une technologie déjà sur le marché (avec marquage CE et/ou FDA) ou pas encore. Dans les deux cas, le développement du dispositif doit être suffisamment abouti pour mener l’évaluation : le développement de [...]

Publié le 09 juin 2020 [...] ication du système d'identification unique des dispositifs médicaux (UDI) dans le cadre des réglementations européenne (2017/745, RDM) et américaine (FDA) oblige les fabricants à identifier et à enregistrer leur produits. L'objectif : un suivi sans faille des produits, une limitation du piratage et une [...]

Publié le 09 juin 2020 [...] . La pièce est réalisée dans un environnement propre non classé, par injection de LSR (Liquid Rubber Silicone) platine USP Class VI, avec un colorant FDA. D’une dureté de 40 Shore A, le silicone a été choisi pour sa qualité, son esthétisme, mais aussi pour sa fiabilité et sa biocompatibilité. Le systèm [...]
Publié le 08 juin 2020 [...] Licensale 2.0. Ils offrent notamment la possibilité d'utiliser le produit d'Arazy pour créer le fichier technique RDM d'un produit ou une application FDA 510K. Rendez-vous sur cette page web pour vous inscrire. Le premier, Licensale, est un système d'enregistrement en ligne tout-en-un. Associ [...]

Publié le 12 mai 2020 [...] et évolutifs. Dans ce sens, la notion même d’"évolution" doit être précisée pour les DMC et harmonisée pour l’ensemble des instances internationales (FDA, HAS). Bien que les RCT ne permettent pas, durant leur cours, d’intégrer des évolutions de systèmes en fonction des retours utilisateurs, il est tout [...]

Publié le 04 mai 2020 [...] iques issues de DM d'imagerie - La transformation numérique en France - Le silicone liquide au service d'un DM de rééducation périnéale connecté - La FDA à l'affût des failles de sécurité. Suisse : Comment augmenter la productivité de votre atelier d'usinage ? - La Suisse considérée comme un Etat ti [...]
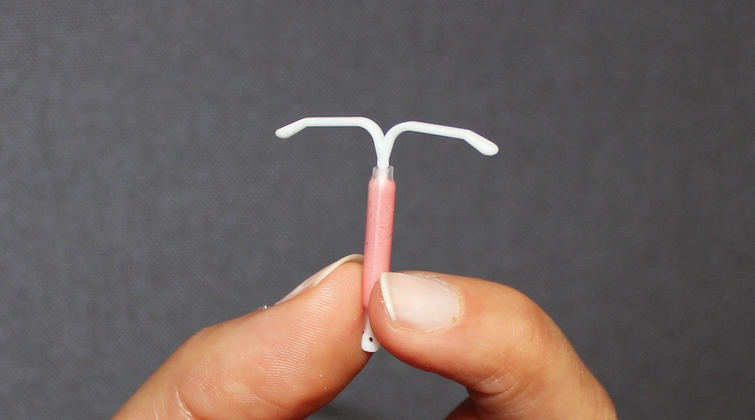
Publié le 23 avril 2020 [...] Enfin, tous les dispositifs combinés d'administration de médicament sont soumis à l'approbation d’organismes de réglementation comme par exemple la FDA, même si le médicament a déjà obtenu cette approbation sous une autre forme. Imprégnation du silicone vulcanisé L'ajout d'API à un composant en [...]
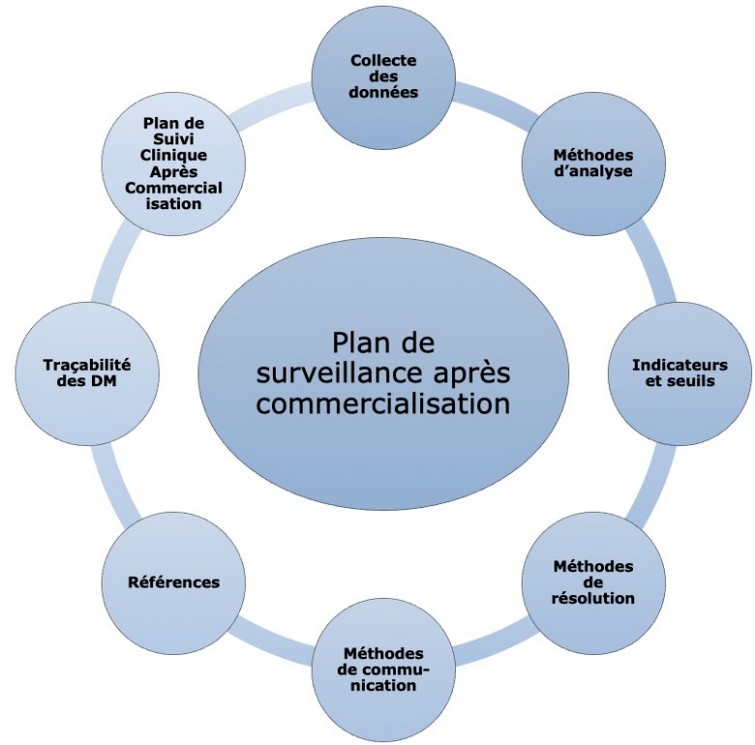
Publié le 14 avril 2020 [...] u plan de surveillance post-commercialisation, et un outil de suivi d'efficacité. Basé à la fois sur le RDM et d’autres sources telles que l’ANSM, la FDA ou le guide MEDDEV 2.12/1 rev8, le premier outil se présente sous la forme d'un document PowerPoint ou PDF regroupant les étapes clés. Par un simple [...]

Publié le 20 mars 2020 [...] angue anglaise. La vidéo du webinaire est en libre consultation. En vertu du Règlement européen 2017/745/UE et de la réglementation imposée par la FDA, les fabricants de dispositifs médicaux sont tenus d’identifier et de faire enregistrer leurs produits selon le système d’identification unique UDI. [...]

Publié le 19 mars 2020 [...] VO-EU- W Réglementation améri- mercialisés aux USA : 21 apprenants. eg ROPE intervient spécifique- caine (FDA) des DM CFR 820 www.cvo-europe.com [...]
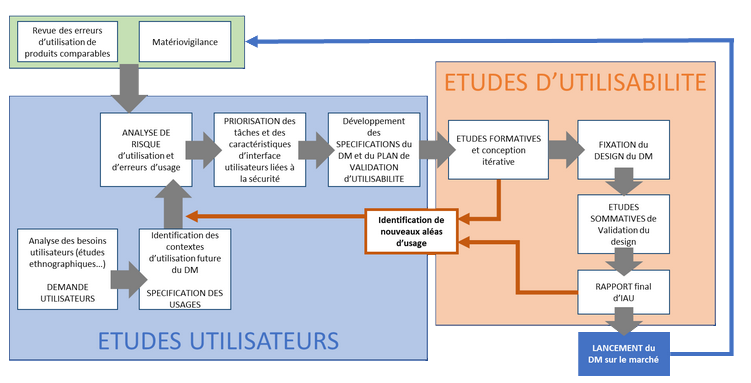
Publié le 17 mars 2020 [...] t répondant aux attentes des autorités. Par Aline Abravanel, Chef de projet international, membre du groupe AFCROs-DM Bien qu’exigée par la FDA et obligatoire en Europe depuis 2010 (Directive 2007/47/EC sur les dispositifs médicaux), l’approche HFE (Human Factor Engineering) est encore mal co [...]

Publié le 11 février 2020 [...] DM représente un investissement important, avec des dépenses estimées à plus de 5 M€ par un tiers des fabricants. Et comme pour l’UDI instauré par la FDA, le respect du RDM exige un effort continu. Plus des deux tiers des répondants déclaraient ne pas avoir de stratégie concernant cet aspect continu de [...]
Publié le 22 janvier 2020 [...] réglementaires les plus strictes EUDAMED, mettre en place tiendra du 21 au 23 avril 2020 tion et propose une offre inté- (marquage CE, FDA, ANVI- une bonne gestion des master à Berlin. Cet événement, qui grée, du prototypage jusqu’au SA...). data de son DM dans le but de [...]

Publié le 20 janvier 2020 [...] de la formulation. Ils sont conformes au règlement UE n° 10/2011 et remplissent les exigences du Code of Federal Regulations, Title 21 (CFR 21) de la FDA. Certifiés selon les normes ISO 10993-5 et -11 pour la biocompatibilité, ces matériaux peuvent être stérilisés aux rayons bêta ou gamma ou à l'EtO. [...]

Publié le 08 novembre 2019 [...] ssage avec succès de l’audit pour la demande d’extension d’accréditation Cofrac pour la validation de nettoyage de DM. Enregistrement auprès de la FDA du groupe et de sa plateforme d’analyses structurales. Cet enregistrement présente un avantage important pour les sociétés présentes sur le marché US [...]

Publié le 08 novembre 2019 [...] l'Espagne (3 %), de la France (2 %) et de l'Allemagne (1 %). « Ces dernières années ont été remarquables en ce qui concerne les approbations de la FDA, mais ce que nous constatons désormais, c'est que ce pipeline de nouveaux médicaments a contribué à stimuler l'innovation dans le domaine de l'emball [...]
Publié le 04 novembre 2019 [...] afin timidement pour les dispositifs médicaux, où seule ropéen, en précisant les activités de gestion des d’écarter tout la FDA s’est risquée à proposer des guides. Notons risques définies dans l’ISO 14971. Or, cette dernière conflit d’intérêt, que cette nor [...]

Publié le 29 octobre 2019 [...] guides chirurgicaux), ont été validées par Materialise pour être utilisées avec le logiciel Materialise Mimics inPrint. Celui-ci a été reconnu par la FDA pour créer des modèles anatomiques destinés aux soins des patients. La société a travaillé en étroite collaboration avec la Veterans Health Administr [...]

Publié le 29 octobre 2019 [...] 2012 et finalement cédée à son management en 2013. Basée en Suisse, la production répond aux exigences réglementaires les plus strictes (marquage CE, FDA, ANVISA...). « Mediliant est une très belle base pour construire un groupe leader dans la fabrication d’implants orthopédiques. Nous avons été séd [...]
Publié le 14 octobre 2019 [...] e Plastics (MGP) pour élaborer une norme commune pour les matières plastiques de qualité médicale. En effet, malgré les Drug Master Files (DMF) de la FDA aux États-Unis, l’ISO 10993 sur la certification biologique, et le règlement (UE) 2017/745, il n’existait jusqu’alors aucune directive ou norme clair [...]
Publié le 30 septembre 2019 [...] lisations. Il s’agit de procédés validés, « utilisés pour rendre un instrument précédemment utilisé ou contaminé, apte à un usage unique ultérieur » (FDA Reprocessing Guideline:2015). Ces procédés doivent non seulement éliminer les souillures et les contaminants par nettoyage mais également inactive [...]

Publié le 10 septembre 2019 [...] uvrage déléguée », précise aussi obtenir les certifications exigées par le marché Frédéric Obscur. médical (ISO 13485 et FDA 21 CFR part 820). Cela lui Concrètement, il s'agit d’intégrer un maximum a permis de gagner de nouveaux donneurs d'ordres d’opér [...]

Publié le 12 août 2019 [...] compte d’un état de l’art particulièrement développé en pharmacie, en médecine et beaucoup plus timidement pour les dispositifs médicaux, où seule la FDA s’est risquée à proposer des guides. Notons que cette norme ne sera ni harmonisée, ni d’application obligatoire. Ceci dit, une norme nationale peut t [...]

Publié le 08 août 2019 [...] on à découvrir très prochainement… Albhades ainsi que sa plateforme d'analyses structurales bénéficient également d'un enregistrement auprès de la FDA. Cet enregistrement présente évidemment un avantage déterminant pour les sociétés présentes sur le marché américain. Avec une croissance du chiffr [...]

Publié le 08 août 2019 [...] en Bradley, certifié SIL selon IEC 61508, son propre système de contrôle basé sur la technologie SCADA et conforme à la norme 21 CFR Part 11 de la FDA. Enfin, RSD se charge de générer et d’exécuter les protocoles de qualité, ce qui garantit au client la conformité réglementaire de l’équipement.

Publié le 22 juillet 2019 [...] par une presse électrique Allrounder 370 A en version inox qui satisfait aux exigences de la norme ISO 13485 en matière d'hygiène, aux spécifications FDA et aux directives GMP (bonnes pratiques de fabrication). Le temps de cycle était de 26 secondes environ. Un module d'air pur avec ionisation situé au [...]

Publié le 08 juillet 2019 [...] angement fera la différence. 1 A Survey over 200 medical technology companies, Josh MAKOWER, Stanford University, 2010 2 Drugs, Devices, and the FDA: Part 2: An Overview of Approval Processes, Gail A.Van Norman, 2016 3 Sécuriser et optimiser les budgets de développement des projets dans l’aérona [...]

Publié le 04 juillet 2019 [...] Par ailleurs, GVS propose et les bactéries. pr douleur, hémodialyse, chirur- ISO 13485 et FDA. une gamme de régulateurs de www.gvs.com 42 [...]
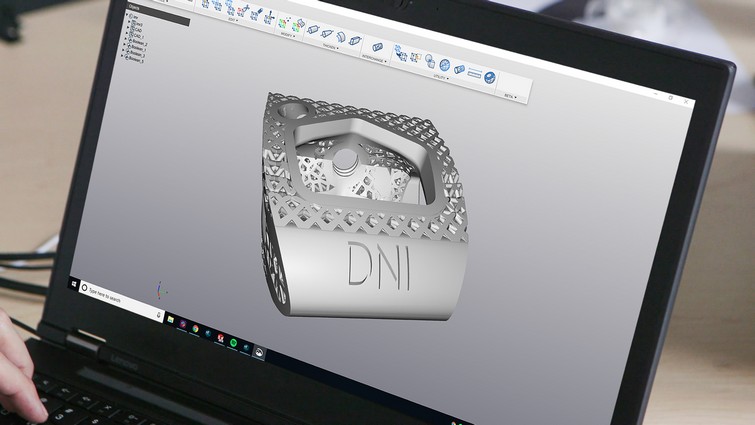
Publié le 13 mai 2019 [...] ntreprise a réalisé une série de tests pour démontrer que le dispositif répondait aux critères les plus pertinents des spécifications énoncées par la FDA. Les propriétés chimiques ont été testées pour garantir la conformité aux normes ASTM F136 (spécification du titane forgé de grade 23 employé [...]

Publié le 13 mai 2019 [...] tres partenaires et soutiens s’engageront auprès de France Biotech pour promouvoir la HealthTech. Pour les dispositifs médicaux déjà marqués CE ou FDA L’organisation de cette journée dans l’Hexagone traduit la volonté de France Biotech d’accompagner les entreprises françaises et européennes dan [...]
Publié le 10 mai 2019 [...] u l’homologation de technologies en santé Cette initiative a pour objectif de renforcer le dia- FDA. logue entre les OTT et les entrepreneurs de l’inno- Suite aux travaux initiés par le groupe de travail vation en santé [...]

Publié le 02 avril 2019 [...] 017, l'entreprise a vendu près de 1350 tonnes de fil dont la majeure partie sur le marché des dispositifs médicaux. Elle est enregistrée auprès de la FDA et certifiée ISO 9001, AS 9100D et ISO 13485. Réputé pour son esprit d'innovation, Fort Wayne s'applique à développer de nouveaux alliages et maté [...]

Publié le 05 mars 2019 [...] ais aussi dans le cadre des essais cliniques menant à l’approbation des DM auprès des autorités compétentes. C’est là un point critique sur lequel la FDA américaine a pris les devants, en encoura- geant les essais numériques depuis quelques années déjà. C'est ainsi que Medtronic et Johnson & Johnson, [...]

Publié le 28 janvier 2019 [...] ve beaucoup d’interrogations, voire d’inquiétudes. Dans le secteur du DM, l’une des principales questions concerne la sécurité. Aux États-Unis, la FDA a autorisé la mise sur le marché du logiciel IDx-DR, qui utilise un algo- rithme d’IA pour dépister les rétinopathies. Il y a de quoi être surpris qu [...]
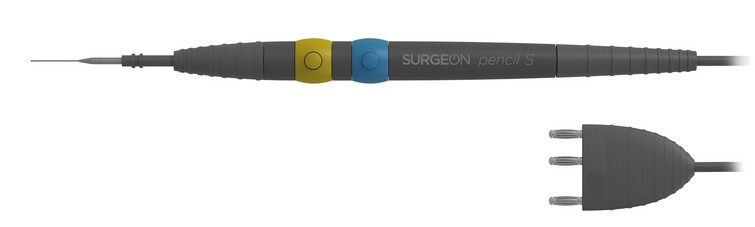
Publié le 21 janvier 2019 [...] ais peut être teint sur demande sans perdre son homologation de base pour les usages médicaux. Par ailleurs, un Drug Master File est conservé à la FDA pour toutes les références de la gamme Thermolast M afin de garantir au fabricant de DM la formulation spécifiée et le processus de fabrication. Tous [...]

Publié le 07 janvier 2019 [...] atives d’aptitude à l’utilisation ? présente l’approche théorique constituant l’état de l’art, utilisée dans le guide IEC 62366-2 et dans celui de la FDA dédié à l’ingénierie de l'aptitude à l'utilisation (IAU), pour enfin savoir combien d’utilisateurs enrôler. Un autre, intitulé (in)aptitude à l’ut [...]

Publié le 20 novembre 2018 [...] Recommandation de la EN 62366:2008 2011 FDA : codes UDI (Unique

Publié le 19 novembre 2018 [...] répondant à des besoins techniques ou esthétiques. Un panel de couleurs est dorénavant disponible, pour des matières répondant aux exigences qualité FDA ou de grade médical USP classe VI. Initialement développé pour le prototypage rapide, le procédé SiO-shaping permet désormais d’imprimer de la pet [...]

Publié le 12 novembre 2018 [...] Recommandation de la EN 62366:2008 2011 FDA : codes UDI (Unique

Publié le 30 octobre 2018 Face au besoin d'un fabricant de pompes de nutrition entérale devant répondre aux exigences de la FDA, Emitech a développé un banc d'essai spécifique pour tester les DM aux fréquences en dessous de 150 kHz. Spécialisé [...]

Publié le 30 octobre 2018 [...] numérique pour comprendre, optimiser et valider l’implantation de divers types de dispositifs médicaux. La situation évolue sous l’impulsion de la FDA (Food and Drug Administration) aux États-Unis et de l’Alliance Avicenna en Europe, qui veulent intégrer la simulation numérique à la Réglementation. [...]

Publié le 16 octobre 2018 [...] ité et de qualité des soins. Mais la communication sans fil représente un défi de taille, notamment en termes de cybersécurité. Aux Etats-Unis, la FDA (Food and Drug Administration) a approuvé la première pilule numérique, équipée d'un petit capteur ingérable, dont le but est de s'assurer que le pat [...]

Publié le 02 octobre 2018 [...] glementaire périlleuse, le secteur ayant l’habitude de parler diagnostic, thérapie ou contrôle de processus physiologique. Un positionnement de la FDA particulièrement favorable Document très important pour comprendre le dossier : une lettre de la
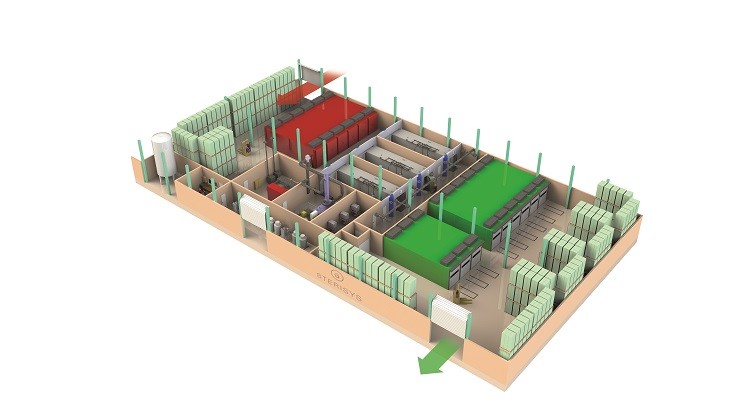
Publié le 17 septembre 2018 [...] az, ainsi que leur propre logiciel de contrôle de process, appelé sysREG. Le logiciel de supervision, développé conformément aux directives GAMP 5 et FDA 21 CFR Part 11, offre la possibilité de surveiller, visualiser et contrôler l'ensemble du procédé de stérilisation. Les installations de stérilisa [...]
Publié le 09 septembre 2018 [...] orthopédiques. Caractériser en France pour vendre aux US Pour coller aux nouvelles exigences de la FDA, Novastep a demandé au Cetim de caractériser la sensibilité à la corrosion d'agrafes compressives et superélastiques pour le pied suivant la norme AS [...]