Recom International

Des générateurs de fumée pour caractériser les flux d’air
Publié le 26 mars 2026

Un interlocuteur unique pour la rectification et le polissage
Publié le 24 mars 2026

Horlogerie et medtech : quand la micro‑précision crée des opportunités au cœur d’EPHJ
Publié le 24 mars 2026

Fluidifier la validation en plasturgie médicale sans compromettre la rigueur
Publié le 17 mars 2026

Les avancées et les orientations futures de la santé connectée
Publié le 17 mars 2026
DeviceMed Mars/Avril 2026
Publié le 17 mars 2026

Comment réaliser son dossier de conception en conformité avec le MDR
Publié le 03 mars 2026

Soigner français grâce à la force de notre écosystème : le credo de MedTech in France
Publié le 17 février 2026

DeviceMed Janvier/Février 2026
Publié le 12 février 2026

1er site européen de stérilisation aux rayons X chez Ionisos
Publié le 03 février 2026
Les atouts des corelabs dans les investigations cliniques
Publié le 22 janvier 2026

Une contraception féminine révolutionnaire grâce à la micro-mécatronique
Publié le 06 janvier 2026

Assurance et DM logiciels : une exigence réglementaire et stratégique
Publié le 06 janvier 2026
Master protocol : pilier de structuration des investigations cliniques
Publié le 24 novembre 2025

DeviceMed Novembre/Décembre 2025
Publié le 06 novembre 2025

Norme IEC 62304 : un périmètre qui va s’étendre aux logiciels de santé
Publié le 28 octobre 2025
Motoriser un DM d’administration de médicament, réutilisable ou non
Publié le 14 octobre 2025

Conformité des DMDIV dits « legacy » au Règlement (UE) 2017/746
Publié le 14 octobre 2025
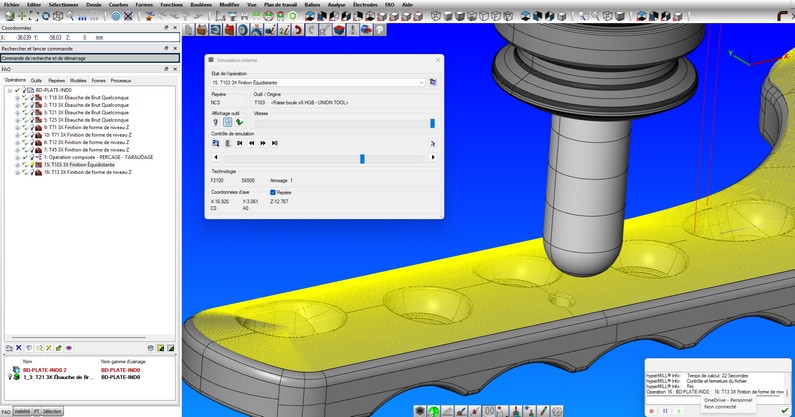
Polis Précis utilise la FAO hyperMILL pour piloter ses machines 5 axes
Publié le 30 septembre 2025

Coveris annonce des scores EcoVadis record pour 24 de ses sites
Publié le 30 septembre 2025

DeviceMed Septembre/Octobre 2025
Publié le 19 septembre 2025

L’IA en réglementaire : providentielle ou nuisible pour les services QA/RA ?
Publié le 16 septembre 2025

Un microrobot conçu à l’aide de Solidworks
Publié le 05 septembre 2025

Injection plastique de pièces médicales en salle propre : un livre blanc gratuit
Publié le 02 septembre 2025

Acrotec parmi les entreprises les mieux gérées de Suisse
Publié le 31 juillet 2025

Règlement MDR : tout savoir pour rédiger un PSUR conforme
Publié le 31 juillet 2025

Faciliter l’accès aux marchés européen et U.S. des DM logiciels de classe II
Publié le 22 juillet 2025

RGPD : enjeux et bonnes pratiques pour les investigations cliniques
Publié le 22 juillet 2025

DeviceMed guide de l’acheteur 2025-2026
Publié le 08 juillet 2025

Une nouvelle offre de formations de la part du LNE et de GMed
Publié le 07 juillet 2025

Etat de la recherche clinique en France dans le DM : le baromètre de l’AFCROs
Publié le 07 juillet 2025

Flinn.ai : l’IA qui libère la MedTech du fardeau réglementaire en France
Publié le 23 juin 2025

Une expertise pointue en impression 3D, de l’horlogerie à la medtech
Publié le 23 juin 2025

La Journée start-up innovantes du DM de retour à Paris
Publié le 13 mai 2025
De l’importance d’anticiper la sécurité biologique des DM dès la conception
Publié le 13 mai 2025
DeviceMed Mai/Juin 2025
Publié le 13 mai 2025
Solutions d’assemblage de dispositifs médicaux par collage
Publié le 14 avril 2025

L’intelligence artificielle : un catalyseur pour la recherche clinique
Publié le 01 avril 2025

Modélisation et simulation sous la perspective réglementaire
Publié le 01 avril 2025

Evaluation clinique des produits sans destination médicale prévue
Publié le 18 mars 2025

DeviceMed Mars/Avril 2025
Publié le 14 mars 2025

Sécuriser les DM connectés : le rôle essentiel du pentest
Publié le 25 février 2025

Digitalisation de la santé : regards croisés IA et cyber
Publié le 18 février 2025

DeviceMed Janvier/Février 2025
Publié le 11 février 2025

Conformité du SMQ d’un « legacy device » aux Règlements (UE) 2017/746 et 2024/1860
Publié le 17 janvier 2025

Identifier et quantifier les produits de dégradation de DM en plastique
Publié le 07 janvier 2025

Formation continue : un levier d’éco-responsabilité en santé
Publié le 07 janvier 2025

Loi IA et DM : une approche globale fondée sur la maîtrise des risques
Publié le 07 janvier 2025

Comment mener l’évaluation clinique d’un logiciel dispositif médical ?
Publié le 12 novembre 2024

DeviceMed Novembre/Décembre 2024
Publié le 05 novembre 2024




























