CG.Tec Injection
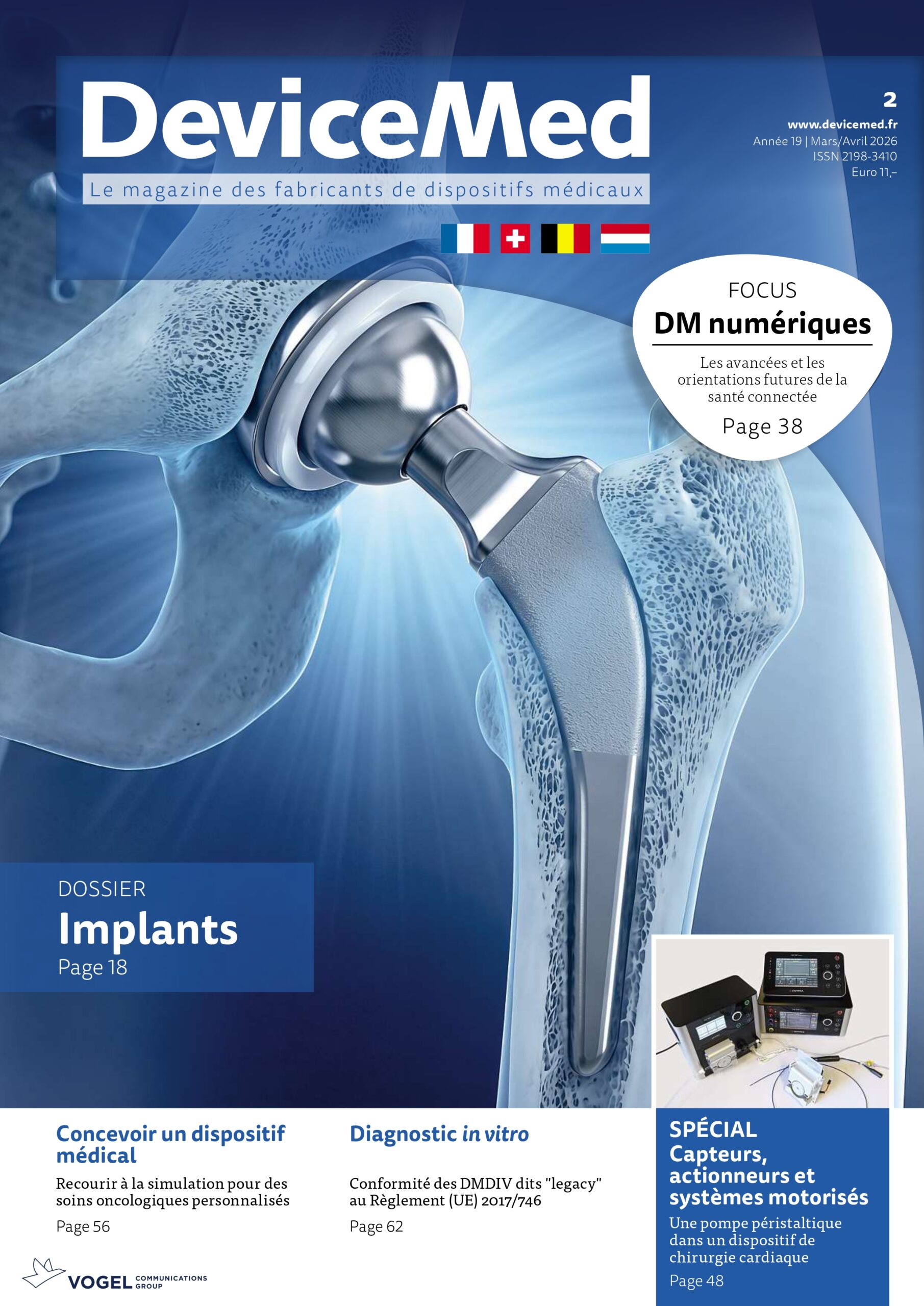
DeviceMed Mars/Avril 2026
Publié le 17 mars 2026

Dispositifs implantables actifs : enjeux et trajectoires
Publié le 26 février 2026

MedTech Meetup le 31 mars 2026 à La Rochelle
Publié le 17 février 2026

DeviceMed Janvier/Février 2026
Publié le 12 février 2026

Webinaire sur la gestion de production de DM le 11 février 2026
Publié le 03 février 2026
Les atouts des corelabs dans les investigations cliniques
Publié le 22 janvier 2026

Communication en champ proche : les atouts du mmWave pour l’e-santé
Publié le 20 janvier 2026

Fonctionnaliser la surface des pièces plastiques pour en maîtriser l’apparence
Publié le 13 janvier 2026

Evaluation clinique : retour sur la journée AFCROs & DM 2025
Publié le 09 décembre 2025
CGR International
Publié le 26 novembre 2025

Une pompe péristaltique dans un dispositif d’« ablation » cardiaque
Publié le 24 novembre 2025

Medtech en Allemagne : une reprise timide cette année ?
Publié le 13 novembre 2025

DeviceMed Novembre/Décembre 2025
Publié le 06 novembre 2025

Conformité des DMDIV dits « legacy » au Règlement (UE) 2017/746
Publié le 14 octobre 2025
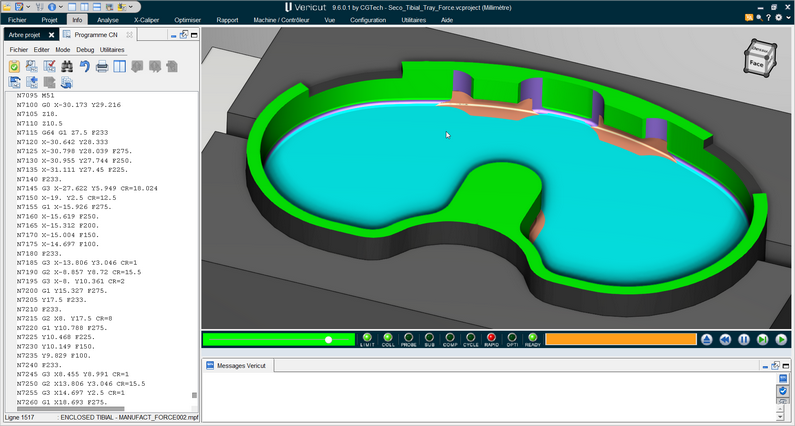
De l’intérêt de simuler et optimiser l’usinage des implants orthopédiques
Publié le 14 octobre 2025

Investigations cliniques en médecine esthétique selon l’annexe XVI du RDM
Publié le 14 octobre 2025
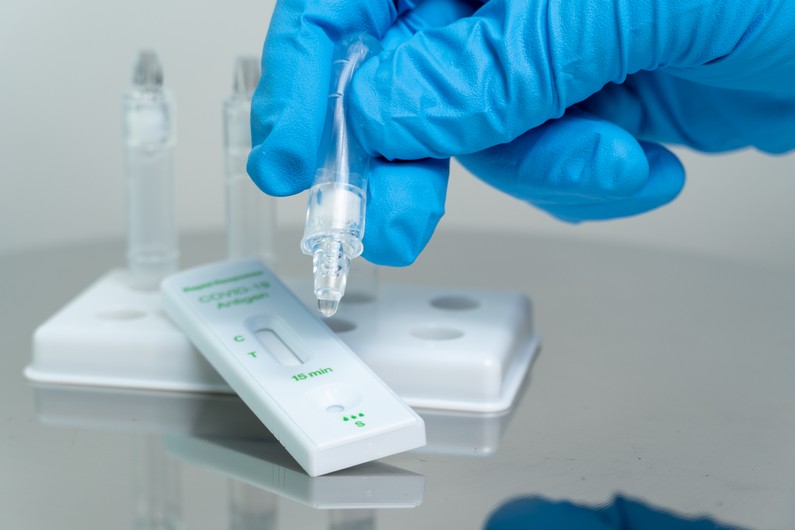
SGS propose une offre complète pour la certification des DM DIV
Publié le 30 septembre 2025

DeviceMed Septembre/Octobre 2025
Publié le 19 septembre 2025

Règlement MDR : tout savoir pour rédiger un PSUR conforme
Publié le 31 juillet 2025

DeviceMed guide de l’acheteur 2025-2026
Publié le 08 juillet 2025
DeviceMed Mai/Juin 2025
Publié le 13 mai 2025

Modélisation et simulation sous la perspective réglementaire
Publié le 01 avril 2025

DeviceMed Janvier/Février 2025
Publié le 11 février 2025

Conformité du SMQ d’un « legacy device » aux Règlements (UE) 2017/746 et 2024/1860
Publié le 17 janvier 2025

Evaluation clinique : retour sur la journée AFCROs & DM 2024
Publié le 10 décembre 2024

Comment mener l’évaluation clinique d’un logiciel dispositif médical ?
Publié le 12 novembre 2024

DeviceMed Novembre/Décembre 2024
Publié le 05 novembre 2024

PMS et matériovigilance : une incitation à la coopération entre fabricants et distributeurs
Publié le 01 octobre 2024

DeviceMed Septembre/Octobre 2024
Publié le 09 septembre 2024

DeviceMed guide de l’acheteur 2024-2025
Publié le 10 juillet 2024

La 3ème édition du TEAM-PRRC Annual Summit sera espagnole !
Publié le 25 juin 2024
Comment évaluer les extractibles et les relargables d’un DM combiné ?
Publié le 14 mai 2024
DeviceMed Mai/Juin 2024
Publié le 30 avril 2024

Peut-on être responsable QARA et garder le moral ?
Publié le 23 avril 2024

RDM : comment gérer les évènements de sécurité dans le cadre d’une IC ?
Publié le 23 avril 2024

Evaluation clinique des DM : retour sur la journée AFCROs & DM 2023
Publié le 18 mars 2024

DeviceMed Mars/Avril 2024
Publié le 12 mars 2024

DeviceMed Janvier/Février 2024
Publié le 05 février 2024

Petit, précis, complexe et écologique : les points forts de Demgy Frasne
Publié le 25 septembre 2023
Investigation clinique : le secteur de la cardiologie montre l’exemple
Publié le 19 septembre 2023

DeviceMed Septembre/Octobre 2023
Publié le 05 septembre 2023

Evaluation clinique : retours d’expérience d’un organisme notifié
Publié le 01 septembre 2023

DeviceMed guide de l’acheteur 2023-2024
Publié le 17 juillet 2023
Promouvoir la modélisation et la simulation numérique en France
Publié le 06 juin 2023

Comment tester la stabilité de son dispositif médical ?
Publié le 09 mai 2023

DeviceMed Mai/Juin 2023
Publié le 01 mai 2023
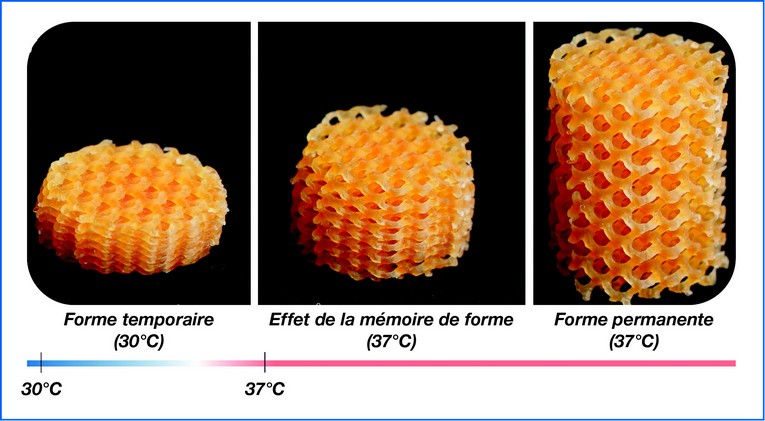
Impression 4D : un avenir prometteur pour la médecine personnalisée
Publié le 25 avril 2023

Etude de faisabilité précoce : un outil pertinent à mettre en place au niveau européen
Publié le 28 mars 2023

Résumé des caractéristiques de sécurité et des performances cliniques
Publié le 13 mars 2023
DeviceMed Mars/Avril 2023
Publié le 06 mars 2023


























