Materialise

DeviceMed Mars/Avril 2024
Publié le 12 mars 2024

Atessia et Ubaq s’associent pour simplifier la gestion réglementaire
Publié le 10 novembre 2023

DeviceMed guide de l’acheteur 2023-2024
Publié le 17 juillet 2023

DeviceMed Mai/Juin 2023
Publié le 01 mai 2023
DeviceMed Mars/Avril 2023
Publié le 06 mars 2023
DeviceMed Novembre/Décembre 2022
Publié le 31 octobre 2022

Convention d’affaires Medtech Meetings le 8 décembre 2022
Publié le 24 octobre 2022

Une solution ERP adaptée aux besoins des entreprises du dispositif médical
Publié le 09 août 2022
DeviceMed guide de l’acheteur 2022-2023
Publié le 01 juillet 2022

Concilier fin des documents papier et mise en conformité
Publié le 23 mai 2022
DeviceMed Mai/Juin 2022
Publié le 25 avril 2022

Virtualisation du SCAC : de multiples intérêts pour les fabricants de DM
Publié le 29 mars 2022
Devicemed Mars/Avril 2022
Publié le 11 mars 2022

Steriservices : 20 ans d’expérience dédiés aux dispositifs médicaux
Publié le 14 décembre 2021
DeviceMed guide de l’acheteur 2021-2022
Publié le 05 juillet 2021
DeviceMed Mai/Juin 2021
Publié le 06 mai 2021

Stérilisation : un suivi de flux entièrement dématérialisé
Publié le 27 avril 2021

La personnalisation serait-elle la clé de soins plus efficaces et moins coûteux ?
Publié le 01 décembre 2020

DeviceMed Novembre/Décembre 2020
Publié le 10 novembre 2020

L’ANSM ouvre un guichet « innovation et orientation »
Publié le 21 septembre 2020

DeviceMed Septembre/Octobre 2020
Publié le 02 septembre 2020

DeviceMed Mars/Avril 2020
Publié le 19 mars 2020
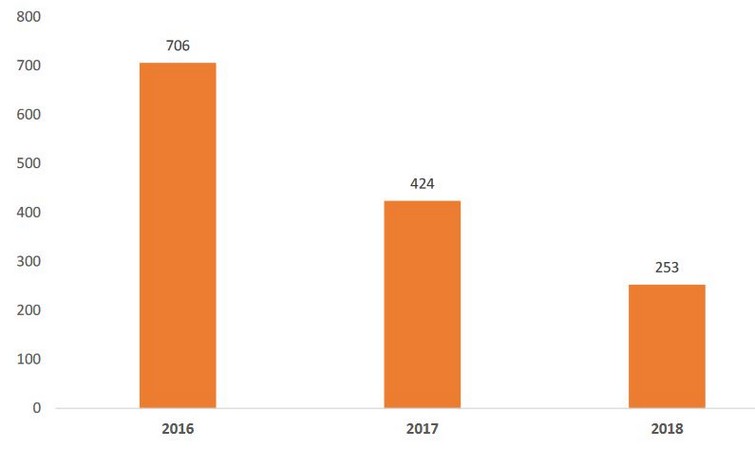
Remboursement de DM : un webinaire de la HAS pour réduire les non-conformités
Publié le 17 février 2020

Une solution dédiée à l’impression 3D de modèles anatomiques réalistes
Publié le 29 octobre 2019

DeviceMed Septembre/Octobre 2019
Publié le 10 septembre 2019

DeviceMed guide de l’acheteur 2019
Publié le 04 juillet 2019
DeviceMed Mai/Juin 2019
Publié le 10 mai 2019

France Biotech propose des solutions concrètes pour fluidifier le transfert technologique
Publié le 14 mars 2019

DeviceMed Janvier/Février 2019
Publié le 28 janvier 2019

Inscriptions sur la « liste en sus » : quel bilan tirer à ce jour ?
Publié le 19 juillet 2018

DeviceMed Juillet/Août 2018
Publié le 10 juillet 2018

DeviceMed Mars/Avril 2018
Publié le 12 mars 2018

DeviceMed Janvier/Février 2018
Publié le 19 janvier 2018

Devicemed Novembre/Décembre 2017
Publié le 06 novembre 2017

Fresenius Vial confie à Cegedim l’envoi de ses factures dématérialisées
Publié le 13 décembre 2016

Nouveau règlement DM : un maillage dense de changements (partie 1)
Publié le 09 septembre 2016

Conférences 2016 de MedPharmaPlast Europe : le 29 juin à Strasbourg
Publié le 23 juin 2016

Top 5 des tendances en matière de test électronique de DM
Publié le 15 mai 2016

Système qualité et conformité réglementaire
Publié le 29 janvier 2015

Le Pôle Santé est sorti de terre
Publié le 18 mars 2014
Un rapprochement qui s’imposait
Publié le 31 octobre 2012

Procédure 510 (k) pour les USA : comment éviter le piège ?
Publié le 12 janvier 2012





























