Guillaume Siantago

Assurance et DM logiciels : une exigence réglementaire et stratégique
Publié le 06 janvier 2026

Orthomanufacture 2024 : un lieu de prestige pour prendre de la hauteur !
Publié le 16 avril 2024

DeviceMed Mars/Avril 2024
Publié le 12 mars 2024

Revival Bionics reste fidèle à maxon pour la V2 de sa prothèse de pied
Publié le 05 mars 2024

Une ligne de nettoyage et de passivation équipée pour la traçabilité
Publié le 06 février 2024

DeviceMed Janvier/Février 2024
Publié le 05 février 2024

L’évaluation biologique des dispositifs médicaux voies de gaz respiratoires
Publié le 31 octobre 2023

DeviceMed Septembre/Octobre 2023
Publié le 05 septembre 2023

Diviser le coût de production en série de biomédicaments par 10
Publié le 30 août 2023

Viant Chaumont : un partenaire solide pour des implants de qualité
Publié le 17 juillet 2023

DeviceMed guide de l’acheteur 2023-2024
Publié le 17 juillet 2023

DeviceMed Mai/Juin 2023
Publié le 01 mai 2023

Quest for health, incubateur du Grand Est dédié aux start-up de la santé
Publié le 14 février 2023
DeviceMed Novembre/Décembre 2022
Publié le 31 octobre 2022

Rapprochement des cabinets de conseil Nextep et SGE Consulting
Publié le 03 octobre 2022
DeviceMed Septembre/Octobre 2022
Publié le 06 septembre 2022
DeviceMed guide de l’acheteur 2022-2023
Publié le 01 juillet 2022

Une huile de coupe adaptée à l’usinage d’implants orthopédiques
Publié le 08 juin 2022
DeviceMed Janvier/Février 2022
Publié le 04 février 2022
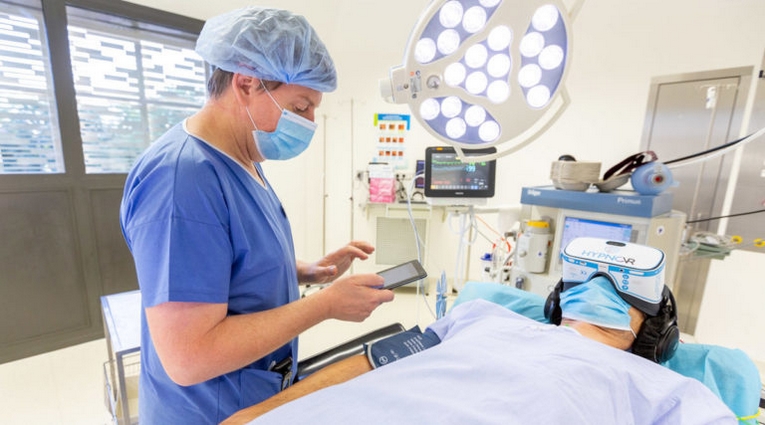
HypnoVR lève 4,5 M€ pour déployer sa thérapie digitale de traitement de la douleur et de l’anxiété
Publié le 21 décembre 2021

Un bel exemple d’engagement face aux enjeux sociaux et environnementaux
Publié le 06 juillet 2021
DeviceMed guide de l’acheteur 2021-2022
Publié le 05 juillet 2021
DeviceMed Mai/Juin 2021
Publié le 06 mai 2021

Disposer d’une couverture financière suffisante au regard du risque produit : une nouvelle obligation
Publié le 16 mars 2021

Le « nouveau » dispositif anti-cadeaux entre en vigueur
Publié le 06 octobre 2020
DeviceMed Novembre/Décembre 2019
Publié le 04 novembre 2019

DM « intelligents » : comment maîtriser les risques de responsabilités ?
Publié le 15 octobre 2019

DeviceMed Septembre/Octobre 2019
Publié le 10 septembre 2019

Bénéfice/risque : une norme expérimentale bientôt publiée par l’Afnor
Publié le 12 août 2019

Réduire les coûts de développement et le time-to-market
Publié le 08 juillet 2019

DeviceMed guide de l’acheteur 2019
Publié le 04 juillet 2019

DeviceMed Janvier/Février 2019
Publié le 28 janvier 2019

Aptitude à l’utilisation : causes classiques d’erreurs et exemples concrets
Publié le 07 janvier 2019

Guide pour les porteurs de projet de dispositif médical
Publié le 11 décembre 2018
Technomimétisme : une alternative au biomimétisme
Publié le 27 novembre 2018

DeviceMed Novembre/Décembre 2018
Publié le 20 novembre 2018

10 ans de DeviceMed – Rétrospective et Perspectives
Publié le 12 novembre 2018

Apple et le dispositif médical : étude d’une « révolution » règlementaire
Publié le 02 octobre 2018

Assurer le risque de perte de marquage CE, c’est désormais possible !
Publié le 17 septembre 2018
DeviceMed Septembre/Octobre 2018
Publié le 09 septembre 2018

De l’art d’optimiser l’usinage d’implants orthopédiques
Publié le 19 mars 2018

Devicemed Novembre/Décembre 2017
Publié le 06 novembre 2017

DeviceMed Guide de l’acheteur 2017
Publié le 04 août 2017

Le marché américain : prometteur quand on sait l’anticiper
Publié le 13 mars 2017

Formation à l’ISO 13485:2016, le 13 décembre à Besançon
Publié le 29 novembre 2016

SMQ : les nouvelles versions des normes ISO 9001 et ISO 13485 sont-elles toujours compatibles ?
Publié le 09 novembre 2015

La puissance d’un groupe au service de l’innovation en plasturgie
Publié le 21 janvier 2014






























