L’expérience patient, partie intégrante des investigations cliniques
Fortement recommandée par les autorités de santé, l’expérience patient doit être intégrée dès les premières phases d’investigation clinique d'un DM, tout comme l’évaluation des performances et de la sécurité, et la prise en compte de l’impact organisationnel. L'AFCROs nous explique comment procéder.
Par Céline Fabre et Morgane Champiot du groupe AFCROs-DM
L'expérience patient est définie comme l'ensemble des interactions et des situations vécues par une personne et son entourage au cours de son parcours santé.
Les Patient Reported Outcome (PROs) constituent un outil d'évaluation du résultat perçu par le patient, sans interprétation du médecin ou d’une tierce personne. Cette approche permet de générer des données pertinentes, fiables et robustes qui font notamment partie des bases d’évaluation des dispositifs médicaux (DM). On distingue :
- les Patient-Reported Outcome Measures (PROMs), qui mesurent des résultats de soin ;
- et les Patient-Reported Experience Measures (PREMs), qui mesurent l’expérience patient concernant son parcours de soin (accès au soin, implication dans la décision…)
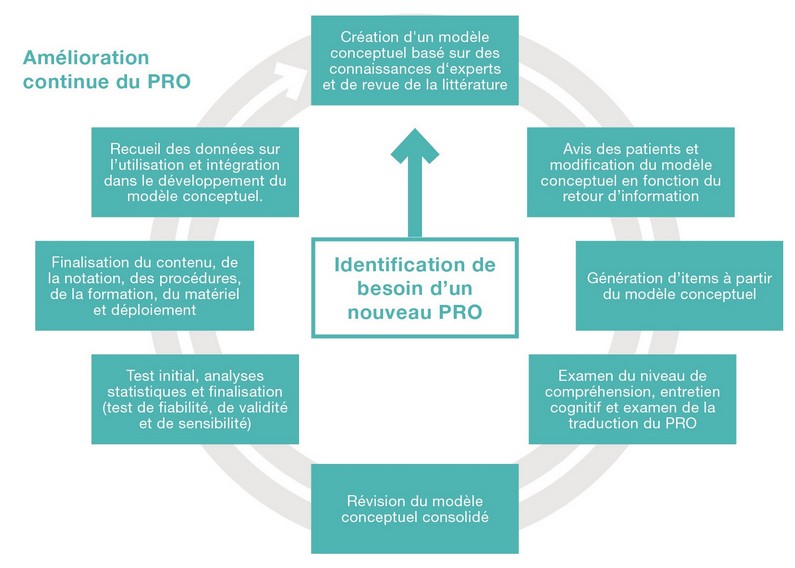
Développement et méthodologie des PROs
En intégrant la voix des patients tout au long du cycle de vie du produit, les concepts importants pour les patients peuvent être pris en compte dans l'évaluation et la surveillance des DM. Les instruments PROs peuvent être utilisés dans toutes les étapes de développement d’un DM, lors des phases pilotes (pour améliorer la conception du DM), des études pivotales (notamment pour anticiper l’accès au marché et la prise en charge du dispositif) mais également dans le cadre des études de surveillance post-commercialisation.
La mise en œuvre d’investigations cliniques intégrant des PROMs et des PREMs nécessite une méthodologie statistique adaptée, dépendant du design de l’étude mais aussi du questionnaire. Il existe différents types de questionnaires :
- les questionnaires génériques : ce sont des instruments mesurant des dimensions du résultat des soins qui sont applicables à toutes les situations cliniques (par exemple, l’EQ-5D pour la qualité de vie). Ces questionnaires peuvent être identifiés à partir d'une revue de la littérature ou d’initiatives (ICHOM : International Consortium for Health Outcomes Measurement, PaRIS : Patient-Reported Indicators Survey, PROMIS : Patient-Reported Outcomes Measurement Information System...)
- les questionnaires spécifiques : ce sont des instruments mesurant des résultats importants pour des populations ciblées ou des dimensions particulières du résultat. Ces questionnaires nécessitent d’effectuer une revue de la littérature existante avec les scores disponibles, des entretiens sociologiques pour identifier les dimensions pertinentes pour les patients, des sélections du meilleur questionnaire avec les patients, et éventuellement des traductions et une validation.
Il est également possible d'effectuer une création ex nihilo de questionnaires grâce à un développement collaboratif : entretiens sociologiques avec les patients pour identifier les items, création du modèle conceptuel de l'instrument (items/dimensions/concept), formalisation des questions et mathématisation des scores / sous-scores.
Ces questionnaires doivent ensuite être testés et validés à l’aide de méthodes statistiques : test pilote, réduction des dimensions (IRT Item Response Theory), modèle de mesure de traits latents psychologiques, fidélité et consistance interne, validité (structure, contenu, apparence et construit) et enfin sensibilité au changement avec la différence minimale cliniquement importante (MCID).
Mise en œuvre
Une fois développés, les PROs doivent être pleinement intégrés à l’étude et le processus de collecte bien identifié. Plusieurs approches sont alors possibles :
- un questionnaire auto-administré en ligne via une interface dédiée alimentant directement la base de données de l’étude. On parle de ePRO (electronic-PRO) qui doit être facilement accessible (en ligne, via un QR code, application dédiée…), agréable et aisé à utiliser pour le patient (rappel de saisie par email, sms, notification…) ;
- un questionnaire auto-administré sur papier avec une retranscription dans la base de données par le centre investigateur (si applicable). Si cette solution n’est pas à privilégier, elle peut être nécessaire sur certaines catégories de patients (patients âgés par exemple…) ;
- des entretiens par le centre investigateur ou un sous-traitant du promoteur de l’étude (face à face, téléphone…)
En conclusion...
Au même titre que l’évaluation de la performance et de la sécurité, et de la prise en compte de l’impact organisationnel, l’expérience patient est à intégrer dès les premières phases d’investigation et dans tout le process de développement et de suivi post-commercialisation d'un DM. Etant donné sa nature de plus en plus multidimensionnelle, elle peut constituer un outil de communication et de différenciation sur un marché concurrentiel.
Références :
- Rapport de la HAS "Qualité des soins perçues par le patient – indicateurs PROMs et PREMs" du 01/07/2021
- Guide méthodologique de la HAS "Études en vie réelle pour l’évaluation des médicaments et dispositifs médicaux" du 10/06/2021
- Guideline de FDA "Principles for Selecting, Developing, Modifying, and Adapting Patient-Reported Outcome Instruments for Use in Medical Device Evaluation" du 26/01/2022







 X (ex Twitter)
X (ex Twitter) LinkedIn
LinkedIn




















