Lipidots : des cargos moléculaires pour la délivrance de médicaments
Les travaux du CEA-Leti sur l'administration de médicaments vont bon train, notamment en ce qui concerne les nanoparticules appelées Lipidots. Ces cargos moléculaires sont à l'origine d'une nouvelle approche vaccinale pour lutter contre le sida, développée en collaboration avec l'INSERM.
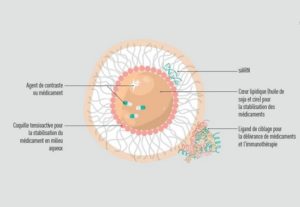
Nanoparticules lipidiques, les Lipidots sont des systèmes colloïdaux présentant un diamètre contrôlé de 50 à 120 nm, fabriqués à partir d’un cœur huileux (mélange de triglycérides saturés et insaturés) encapsulé dans une coquille moléculaire. Cette formulation, qui leur confère des capacités de stockage de molécules actives hydrophobes en milieu aqueux avec une bio-disponibilité accrue, leur permet d’être utilisées comme moyens de transport pour la délivrance de médicaments, par exemple.
Des applications dans l'imagerie par fluorescence à la base
Mis au point en 2006 dans le cadre d’une collaboration entre le CNRS et le CEA-Leti (centre de recherche et technologie spécialisé dans les micro et nanotechnologies du CEA), les Lipidots ont été initialement conçus pour des applications d’imagerie in vivo par fluorescence. Dans ce contexte, il était nécessaire de développer des traceurs présentant des facteurs de brillance de haute qualité tout en présentant des profils de biocompatibilité adéquats pour une future application clinique.
Depuis, ces particules lipidiques ont été extensivement caractérisées d’un point de vue physico-chimique et ont fait l’objet de plusieurs démonstrations précliniques pour des applications en oncologie, allant de l’imagerie de tumeurs solides à la délivrance de molécules thérapeutiques, comme des photosensibilisateurs. Encapsulé dans des Lipidots, le médicament est mieux protégé et n’est délivré que lorsqu'il atteint la cellulle à soigner. L’efficacité du soin est ainsi plus grande et les effets secondaires moins importants.
Vers un nouveau vaccin contre le VIH
Cette approche a notamment permis de mettre au point, en collaboration avec l'INSERM, une nouvelle méthodologie vaccinale basée sur l’administration de la protéine p24, utilisée comme antigène modèle du virus du SIDA. Jusqu’à présent, les vaccins à base de protéine p24 ont fait preuve d’une efficacité limitée en raison d’une réponse immunitaire insuffisante à cet antigène chez les patients atteints du VIH. Le recours aux Lipidots vise à améliorer la réponse immunitaire contre la protéine p24 du VIH en la chargeant avec un agent immunostimulant nommé CpG.
Cette avancée pourrait constituer la première étape vers un nouveau vaccin contre le VIH, auquel seraient ajoutés des composants supplémentaires du virus. Publiés dans la revue npj Vaccines, les résultats chez les souris et les primates non humains valident cette nouvelle approche. Les Lipidots sont en effet capables de protéger l’antigène et l’agent CpG de l'environnement extracellulaire et de procéder à leur délivrance dans les cellules dendritiques, présentatrices d’antigènes et médiatrices des réponses immunitaires induites.
Des Lipidots proches du stade industriel
Les procédés de fabrication des Lipidots ont été mis à l’échelle dans une unité pilote permettant de préparer des larges volumes (> 500 ml) de nanoparticules concentrées et toute la chaîne de caractérisation physico-chimique nécessaire à leur contrôle a été développée. « Nous sommes près d’une transposition au niveau industriel avec un panel applicatif élargi allant de l’imagerie de contraste à la thérapie en passant par la vaccination, », souligne Pascal Mailley, directeur de recherche et directeur scientifique du Département des technologies pour la biologie et la santé au CEA-Leti.
Combiner Lipidots et biopolymères
Si les Lipidots améliorent la délivrance de molécules actives, ils rencontrent des limitations, comme des cinétiques de relargage lentes et difficiles à contrôler. L'encapsulation des nanoparticules dans une matrice appropriée - des hydrogels ou des réseaux de biopolymères biorésorbables - apparaît comme une bonne solution pour mieux contrôler la cinétique de libération de la molécule active.
Différents biomatériaux composites intégrant biopolymères et lipidots ont été élaborés. Il a été démontré qu'il est possible d'incorporer des nanoparticules contenant des fluorophores organiques (utilisés comme modèle de médicament) dans des hydrogels élaborés à partir de carboxyméthyl cellulose (CMC) réticulée par du polyéthylène glycol. La cinétique de libération des nanoparticules peut alors être contrôlée en jouant sur leur diamètre et/ou le taux de réticulation de l’hydrogel.
Dans une autre réalisation, la CMC réticulée a été remplacée par un réseau de polymères interpénétrés, permettant de mieux maîtriser la porosité et les propriétés mécaniques des aérogels formés. Ces différents biomatériaux pourraient être utilisés comme patchs cutanés ou implants post-chirurgicaux afin de favoriser une implantation ou le recouvrement de tissus lésés.
On notera enfin que le CEA-Leti travaille à élaborer des matériaux capables de délivrer des principes actifs de manière minimalement invasive ou implantée. Des micro-aiguilles solubles ont ainsi été réalisées par moulage de polymères biorésorbables tout comme des gels de comblement biorésorbables (destinés à des chirurgies d’exégèse cérébrale suite à des cancers).
La plupart de ces informations sont issues d'un article de Pascal Mailley, paru dans le magazine Clefs N°67 du CEA.





 X (ex Twitter)
X (ex Twitter) LinkedIn
LinkedIn




















