Comment évaluer l’innovation de rupture sur le plan clinique ?
Pour évaluer l’innovation de rupture, le gold standard demeure l'étude clinique comparative, randomisée en double aveugle. Mais il est possible de recourir à une autre méthodologie... sous certaines conditions.
Cet article a été rédigé par Yves Tillet, Audeline Rath-Lavialle, Clément Dubos et Audrey Breysse, du cabinet White Tillet.
Dans le domaine des dispositifs médicaux, qui sont des produits de santé à part entière, on innove pour apporter une amélioration du service rendu aux patients et/ou pour contribuer à une meilleure efficience médico-économique, dans des indications données et pour une population cible bien identifiée. Toutefois, il existe deux types d’innovations : l’innovation incrémentale et l’innovation de rupture. La première réside le plus souvent dans des améliorations, quelquefois substantielles, mais sans rupture technologique ou conceptuelle avec l’existant.
A l’inverse, l’innovation de rupture se caractérise par l’application d’une nouvelle technologie, d’une combinaison nouvelle de technologies, ou d’un nouveau concept. L’innovation de rupture peut atteindre le changement de paradigme. Mais la vraie question reste : comment évaluer au plan clinique l’innovation de rupture ?
Évaluer n'est pas soigner
Derrière cette phrase abrupte se cache une vérité essentielle qui peut choquer un sujet naïf ou néophyte : tout résultat d’évaluation doit être crédible et, pour ce faire, il convient d’utiliser les moyens qui justifient la fin dans les limites de l’éthique. La réponse se trouve essentiellement dans la méthodologie clinique.
L’innovation de rupture, si attractive soit elle, et sauf situation d’urgence ou d’absence d’alternative thérapeutique, s’évalue avec prudence en deux phases, avant la mise sur le marché. Il convient en effet de garantir la sécurité et la performance du nouveau dispositif médical, sans négliger l'aspect médico-économique.

Pour Audeline Rath-Lavialle, tout résultat d’évaluation doit être crédible, ce qui nécessite de choisir la méthodologie clinique adaptée.
La première phase est celle de faisabilité, que la FDA appelle "Horizon screening". Les études de faisabilité sont proposées immédiatement à la suite de la phase pré-clinique. A ce stade, le choix du seuil d’efficacité est primordial. Les études de faisabilité sont utiles pour :
- la mise au point de la technique,
- la mesure de l’efficacité clinique,
- et surtout l’identification des principales complications et des risques.
La phase suivante est celle de la démonstration en vue de la mise sur le marché. A ce niveau, sauf impossibilité dûment justifiée, toute étude doit être comparative, randomisée, et en double aveugle (HAS 2013).
Fiabilité et crédibilité des résultats
Par ailleurs, pour que les données issues de cette comparaison soient fiables, il faut avant tout que les traitements soient attribués de façon aléatoire : c’est la randomisation.
En cas de difficulté, au regard des traitements proposés ou des types de patients (par exemple les enfants), une solution existe ; c’est la randomisation de type “Zelen” ou “Randomised consent design trial”. La randomisation "de Zelen" consiste à randomiser les patients dans les groupes "traitement de référence" et "nouveau traitement" sans avoir préalablement recueilli leur consentement éclairé. Aucun consentement n’est demandé aux patients randomisés dans le groupe "traitement de référence". Seuls les patients randomisés dans le groupe "nouveau traitement" devront signer le consentement éclairé. Si un patient ne consent pas à recevoir le nouveau traitement, il recevra le traitement de référence (HAS 2013).
Durant la phase de faisabilité ou lors des phases précoces de confirmation, on pourra aussi mettre en place une randomisation dite adaptative par laquelle, au début de l’essai, les patients sont randomisés avec un ratio 1:1 dans chaque groupe, puis, à mesure que les résultats commencent à montrer une différence entre les traitements, le ratio est modifié en faveur du groupe qui reçoit le traitement semblant être plus efficace (HAS 2013).
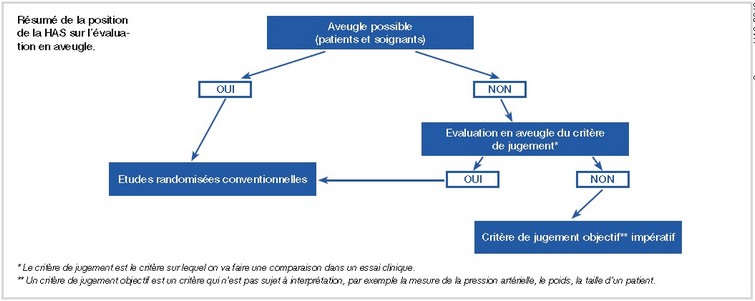
Enfin, pour que le suivi et les résultats de l’étude soient crédibles, il est nécessaire que les patients ainsi que les soignants ignorent quel traitement ils reçoivent ou administrent : c’est le double aveugle. Néanmoins, lorsque cela est impossible, une évaluation dite "en simple aveugle" doit être envisagée. Dans ce cas, l’évaluation est réalisée par des évaluateurs indépendants de l’étude en aveugle du traitement reçu. Cela garantit une évaluation neutre de ce dernier. L’évaluation peut également être centralisée pour des examens biologiques ou radiologiques, ou des extraits de l’examen clinique (vidéo, photos, enregistrement d’entretiens).
En résumé, le gold standard d’un essai clinique visant à démontrer la performance et la sécurité d’un dispositif médical en vue de sa commercialisation reste l’essai comparatif, randomisé en double aveugle. Toute autre méthodologie doit être argumentée au regard des particularités techniques du dispositif médical et de l’objectif de l’étude, en particulier en vue d’éviter les biais et d’assurer la robustesse des résultats de l’essai.
Quels sont les principaux biais à éviter ?
De façon générale, les principaux biais à éviter dans une étude clinique sont les suivants :
- Le biais d'attrition, qui est dû à des différences entre les groupes initiaux et les groupes finaux, liées à des sorties d'essai ou des interruptions de traitement.
- Le biais de confusion qui est consécutif à une erreur d'appréciation entre les effets de la thérapeutique étudiée et les conséquences de la maladie traitée. Le risque de biais de confusion est atténué par l’utilisation d’un groupe-contrôle.
- Le biais de sélection qui est relatif à une différence de composition entre le groupe témoin et le groupe traité.
- Le biais de suivi qui est une conséquence de différences de prise en charge au niveau du groupe traité et du groupe témoin. Par exemple, si le double aveugle n'est pas respecté, il est probable que l'expérimentateur ne suivra pas de la même façon les effets secondaires manifestés par le patient recevant le placebo.
- Le biais d'évaluation qui survient lorsque le critère de jugement n'est pas recherché de la même manière dans les deux groupes. Le risque de biais d'évaluation est supprimé si l'essai est en double insu.
Le nombre d’études à réaliser en phase de faisabilité ou de démonstration dépendra de la complexité de la problématique d’évaluation. Durant la phase de faisabilité, le nombre de patients exposés pourra éventuellement être restreint grâce à l’usage des probabilités conditionnelles (techniques bayésiennes) tandis que dans la phase finale de confirmation la démonstration ne pourra s’établir que par l’usage de la statistique dite fréquentiste (c’est le "p"<0,05 cf. ci-après).
Les bases méthodologiques d'un essai clinique
Selon la statistique fréquentiste, il convient tout d’abord d’établir une hypothèse clinique valide (significative cliniquement et utile médicalement) qui correspond à la question « qu’est-ce que je veux démontrer ? ». Puis, il est nécessaire de fixer les niveaux de risques de faux positif (α) et de faux négatif (β), respectivement et traditionnellement de 5% (p<0,05) et de 10 ou 20 %. Rappelons ici que le risque de faux positif correspond au risque de conclure à l'existence d'une différence qui n'existe pas en réalité, alors qu'à l'inverse, le risque de faux négatif représente le risque de ne pas conclure à une différence qui existe pourtant en réalité.
 Il faut par ailleurs déterminer la différence attendue versus le comparateur (Δ) et la somme des variances (σ) ; ceci généralement à partir d’études antérieures ou de données bibliographiques. L’hypothèse posée prendra en compte les paramètres α, β, Δ, σ afin de déterminer le nombre nécessaire de sujets à inclure dans l’étude de façon à ne pas manquer de vérifier cette hypothèse si elle est vraie. Enfin, il faut choisir le type d’essai que l’on souhaite réaliser :
Il faut par ailleurs déterminer la différence attendue versus le comparateur (Δ) et la somme des variances (σ) ; ceci généralement à partir d’études antérieures ou de données bibliographiques. L’hypothèse posée prendra en compte les paramètres α, β, Δ, σ afin de déterminer le nombre nécessaire de sujets à inclure dans l’étude de façon à ne pas manquer de vérifier cette hypothèse si elle est vraie. Enfin, il faut choisir le type d’essai que l’on souhaite réaliser :
- Étude de supériorité (le produit B est plus efficace que le produit A) ;
- Étude de non infériorité (le produit B n’est pas différent du produit A) ;
- Étude d’équivalence (B et A sont équivalents). Dans une étude de supériorité, le clinicien définira pour le critère principal (critère qui va servir à la mise en évidence de l'efficacité du traitement étudié) la borne supérieure à dépasser pour le nouveau traitement en cas de succès.
Pour une étude de non infériorité, il fixera, pour le critère principal, deux bornes établies de part et d’autre de la moyenne et il ne faudra pas en sortir (sinon ce sera un échec) ; ces bornes seront beaucoup plus resserrées dans une étude d’équivalence.
L'évaluation clinique après mise sur le marché
Dans le cas d’une innovation de rupture, les phases d’évaluation clinique avant mise sur le marché ne sont généralement pas suffisantes pour établir de façon complète la performance et la sécurité, donc le rapport bénéfice/risque du nouveau produit. C’est pourquoi, des études de suivi clinique de post commercialisation sont communément requises, à l’exemple de ce qui suit :
- Complément de démonstration de conformité clinique après apposition du marquage CE pour les produits mis sur le marché par des procédures "accélérées" en raison notamment de la gravité de la pathologie, de l’absence d’alternative, ou de l’intérêt potentiel de l’innovation.
- Vérification de la performance et de la sécurité clinique dans la "vraie vie" pour les produits évalués dans un encadrement trop strict (protocole compliqué très surveillé…) ou trop restreint (essai monocentrique chez un expert).
- Modification substantielle du dispositif innovant avec un impact sur sa performance et sa sécurité cliniques
- Extension de l’indication clinique à une nouvelle population de patients.
Ces études peuvent être, selon les cas, des études de type interventionnelle, de soins courants ou observationnelles.
En conclusion, une innovation de rupture nécessite d’être évaluée avec le plus grand soin, notamment au plan clinique, d’autant que la fonction d’utilité médicale ou médico-économique doit présider à l’allocation des ressources dédiées aux projets innovants, car ces ressources sont aujourd’hui comptées.
Ce ne sont ni la valeur de la découverte scientifique ni la prouesse technique qui doivent emporter la décision "d’entrer en innovation" mais l’intérêt médical à venir, associé à la maîtrise de la qualité du produit.
En effet, pour un produit de santé, le plus important reste de démontrer un rapport bénéfice/risque favorable pour le patient.







 Twitter
Twitter LinkedIn
LinkedIn
























