Vers des implants intra-cérébraux mimétiques ultra-fins et nanostructurés
Le projet Brain Micro Snooper vise à développer une nouvelle génération d'implants intra-cérébraux grâce à des fils flexibles, extrêmement fins, et à des électrodes micro-nanostructurées. Gaëlle Offranc-Piret, qui dirige ce projet, nous explique où il en est et ce qu'on peut en espérer.

Gaëlle Offranc-Piret travaille au sein de l'Unité Inserm U1205 du centre de recherche Braintech à Grenoble dont les activités sont réparties sur les sites du CEA-Leti, de l’université UGA et de l’hôpital CHUGA. Elle collabore avec l’ESIEE à Paris, le LAAS à Toulouse, et l’ESME à Gardanne.
Par Gaëlle Offranc-Piret, Chargée de Recherche à l’INSERM
Le développement des implants cérébraux est crucial pour mieux enregistrer puis déchiffrer les informations neuronales et intervenir très finement sur les réseaux neuronaux en utilisant la microstimulation. Il s'agit de traiter ou palier les dysfonctionnements du système nerveux central et les pathologies associées. Ces dysfonctionnements peuvent être traumatiques, psychologiques, neurodégénératifs, ou en lien avec les tumeurs.
S'adapter à l'environnement cérébral
Transversal, entre ingénierie et biologie, le projet Brain Micro Snooper bénéficie depuis août 2015 d’un financement européen ERC Starting Grant sur 5 ans. Ses deux défis majeurs sont de réaliser un implant mécaniquement stable, permettant une connexion à long terme entre les neurones et les micro-électrodes, puis de fournir des implants neuronaux avec une résolution temporelle et spatiale élevée. L’idée, pour atteindre ces objectifs, est de mettre au point des implants dotés de propriétés structurelles et mécaniques similaires à celles de l’environnement cérébral, donc avec des matériaux souples. Mais ces implants doivent également comporter des dimensions très fines, aux moins dans deux dimensions. On cherche à se rapprocher de la géométrie d’un axone qui a un diamètre de moins d’un micron mais une longueur de plusieurs microns. Il a été montré que plus les électrodes et les fils électriques sont petits, meilleure est la reconstruction du tissu neural autour de l'implant.
A l'heure actuelle, le décalage mécanique entre le matériau d'implant habituellement rigide (Module d’Young d'environ 100 GPa) et le tissu cérébral mou (1 à 10 KPa) et élastique affecte l'adhésion et la qualité de l’interface entre les cellules tissulaires et les électrodes. D'autant plus que le cerveau est irrigué par des artères et qu’il bouge avec les battements du cœur ou les mouvements de notre tête.
Le but est donc d'implanter un réseau de microélectrodes flottant hautement flexible dans le tissu cérébral. Pour cela, les implants développés ici utilisent des étapes de micro-nanotechnologie et des techniques permettant ensuite de manipuler et connecter ces implants ultra-fins et souples.

Implants souples (représentés en bleu), de dimension 1 mm par 10 µm par 10 µm dans un réseau de neurones en noir.
En phase d'études pré-cliniques
Durant ces 3 dernières années, l'équipe de cinq personnes travaillant sur le projet a finalisé les principaux aspects de la fabrication des implants (modules de 64 à 256 micro-électrodes), leur assemblage avec une électronique sans-fil, les études de biocompatibilité in vitro et la méthode chirurgicale pour insérer les implants. Cette dernière étape était risquée, compte tenu des dimensions des fils mous de l'implant. L'équipe de chercheurs est désormais en mesure de les encapsuler dans un matériau biodégradable qui facilite leur implantation puis se résorbe progressivement. Il est aussi possible d'utiliser une navette rigide sur laquelle l'implant est collé avec du polyéthylène glycol (PEG). Le PEG se dissolvant dans les tissus, la navette peut être retirée et l'implant reste dans les couches corticales. Le projet est désormais arrivé au stade des études pré-cliniques dans l’espoir de valider les performances de ces implants en enregistrement in vivo et donc leur utilisation en clinique par la suite.
Le financement européen de ce projet a permis de rassembler un personnel bénéficiant de compétences complémentaires et d’un parcours transversal ; ce qui favorise la communication, la compréhension et l'intégration des contraintes imposées par les technologies, la complexité des systèmes biologiques et les techniques chirurgicales.
Les dispositifs intra-corticaux qui existent en clinique permettent aux individus tétraplégiques, après un long apprentissage, de déplacer un bras robot imitant les mouvements auxquels ils pensent. Des individus ayant le syndrome d’enfermement (conscients avec un retour visuel, mais incapables de bouger ou parler), ont également pu communiquer en cliquant sur des lettres sur un écran. Là aussi l’implant recueille les signaux cérébraux qui traduisent la volonté de la personne.
Pour des traitements plus efficaces
Avec ces implants de nouvelle génération, il deviendrait possible de concevoir la capture et la réalisation de commandes cérébrales plus complexes, et de réduire le temps de l’apprentissage à utiliser ces interfaces cerveau-machines. Ces implants pourraient aussi permettre un modèle plus précis de stimulation neuronale afin d'améliorer certains traitements de pathologie cérébrale utilisant des prothèses neurales (rétine par exemple).

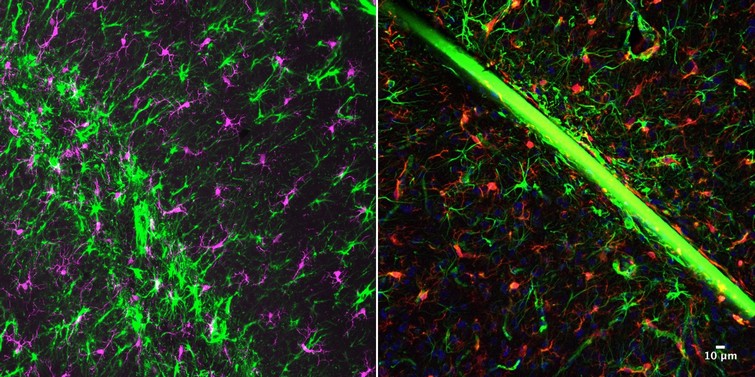
Les nanostructures (ici de diamant dopé) au niveau de l'électrode peuvent favoriser la croissance des neurites tout en limitant la prolifération des cellules gliales. Elle offrent aussi une plus grande surface d'échange pour les charges (électroniques, ioniques).
L'équipe espère donc que l'implant de nouvelle génération, grâce à ses fils flexibles et extrêmement fins d’une part et à ses électrodes micro-nanostructurées d’autre part, sera mieux toléré, ce qui minimisera la formation de tissu cicatriciel. En effet, la littérature et les études préliminaires indiquent que certains nanomatériaux (chimies de surface et nano-topographies spécifiques) peuvent favoriser la croissance des neurites tout en limitant la prolifération des cellules gliales susceptibles d'isoler électriquement les implants. De plus, les électrodes micro-nanostructurées auront une plus grande surface d'échange pour les charges (électroniques, ioniques), ce qui devrait améliorer leur capacité à enregistrer des signaux neuronaux par rapport à des électrodes de rugosité de surface faible ou nulle.
Les challenges restants sont notamment de réduire encore les dimensions de l’implant, d’améliorer ses électrodes micro-nanostructurées et d'incorporer les matériaux qui offrent actuellement les meilleures performances (par exemple le platine, le diamant dopé, le graphène).





 Twitter
Twitter LinkedIn
LinkedIn
























