CG.Tec Injection

Evaluation clinique des DM : retour sur la journée AFCROs & DM 2023
Publié le 18 mars 2024

DeviceMed Mars/Avril 2024
Publié le 12 mars 2024

DeviceMed Janvier/Février 2024
Publié le 05 février 2024

Petit, précis, complexe et écologique : les points forts de Demgy Frasne
Publié le 25 septembre 2023
Investigation clinique : le secteur de la cardiologie montre l’exemple
Publié le 19 septembre 2023

DeviceMed Septembre/Octobre 2023
Publié le 05 septembre 2023

Evaluation clinique : retours d’expérience d’un organisme notifié
Publié le 01 septembre 2023

DeviceMed guide de l’acheteur 2023-2024
Publié le 17 juillet 2023
Promouvoir la modélisation et la simulation numérique en France
Publié le 06 juin 2023

Comment tester la stabilité de son dispositif médical ?
Publié le 09 mai 2023

DeviceMed Mai/Juin 2023
Publié le 01 mai 2023
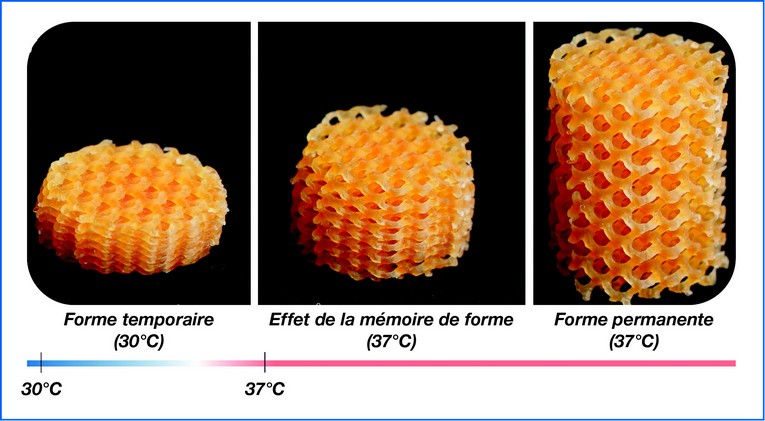
Impression 4D : un avenir prometteur pour la médecine personnalisée
Publié le 25 avril 2023

Etude de faisabilité précoce : un outil pertinent à mettre en place au niveau européen
Publié le 28 mars 2023

Résumé des caractéristiques de sécurité et des performances cliniques
Publié le 13 mars 2023
DeviceMed Mars/Avril 2023
Publié le 06 mars 2023

Vers des emballages rigides écologiques et durables
Publié le 14 février 2023

Une action européenne coordonnée face aux pénuries de dispositifs médicaux
Publié le 31 janvier 2023
DeviceMed Janvier/Février 2023
Publié le 23 janvier 2023

Artificial Intelligence Act : un nouveau règlement européen à suivre de près
Publié le 29 novembre 2022

Forum DMDIV le 24 novembre 2022 en ligne
Publié le 14 novembre 2022
DeviceMed Novembre/Décembre 2022
Publié le 31 octobre 2022

Une stratégie d’usinage repensée au sein du Groupe Lépine
Publié le 18 octobre 2022

3D PRINT revient à Paris les 19 et 20 octobre 2022
Publié le 03 octobre 2022

Comment apporter une preuve clinique suffisante pour se conformer au RDM ?
Publié le 20 septembre 2022
DeviceMed Septembre/Octobre 2022
Publié le 06 septembre 2022
DeviceMed guide de l’acheteur 2022-2023
Publié le 01 juillet 2022

Exercer la fonction de PCVRR : où en sommes-nous aujourd’hui ?
Publié le 08 juin 2022

Concevoir des DM à porter sur soi pour la surveillance des signes vitaux
Publié le 23 mai 2022
DeviceMed Mai/Juin 2022
Publié le 25 avril 2022

IUD : quels leviers pour une mise en conformité efficiente ?
Publié le 21 avril 2022

Virtualisation du SCAC : de multiples intérêts pour les fabricants de DM
Publié le 29 mars 2022
Tests COVID-19 : un point sur la règlementation à l’approche du 26 mai
Publié le 15 mars 2022
Devicemed Mars/Avril 2022
Publié le 11 mars 2022
DeviceMed Janvier/Février 2022
Publié le 04 février 2022

Les dangers liés au MDR : la profession tire la sonnette d’alarme !
Publié le 01 février 2022
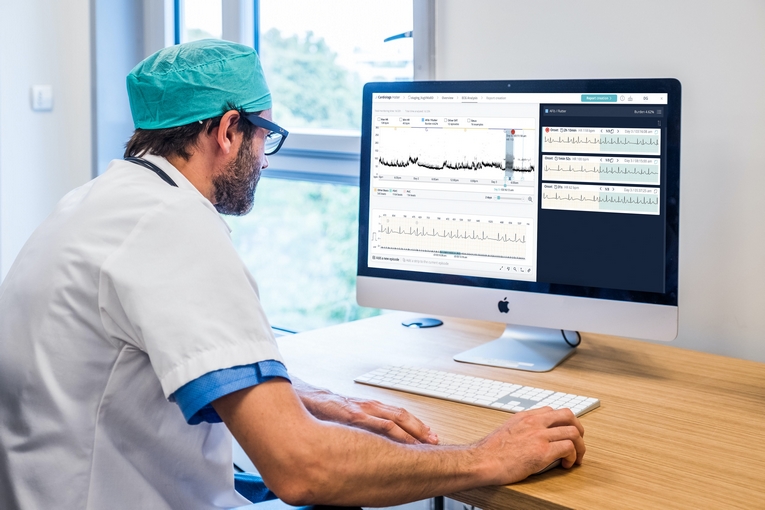
Diagnostic et surveillance cardiaques : Philips s’offre la pépite française Cardiologs
Publié le 21 décembre 2021

Que disent les règlements européens sur les DM face aux défis de l’IA ?
Publié le 08 novembre 2021
DeviceMed Novembre/Décembre 2021
Publié le 03 novembre 2021
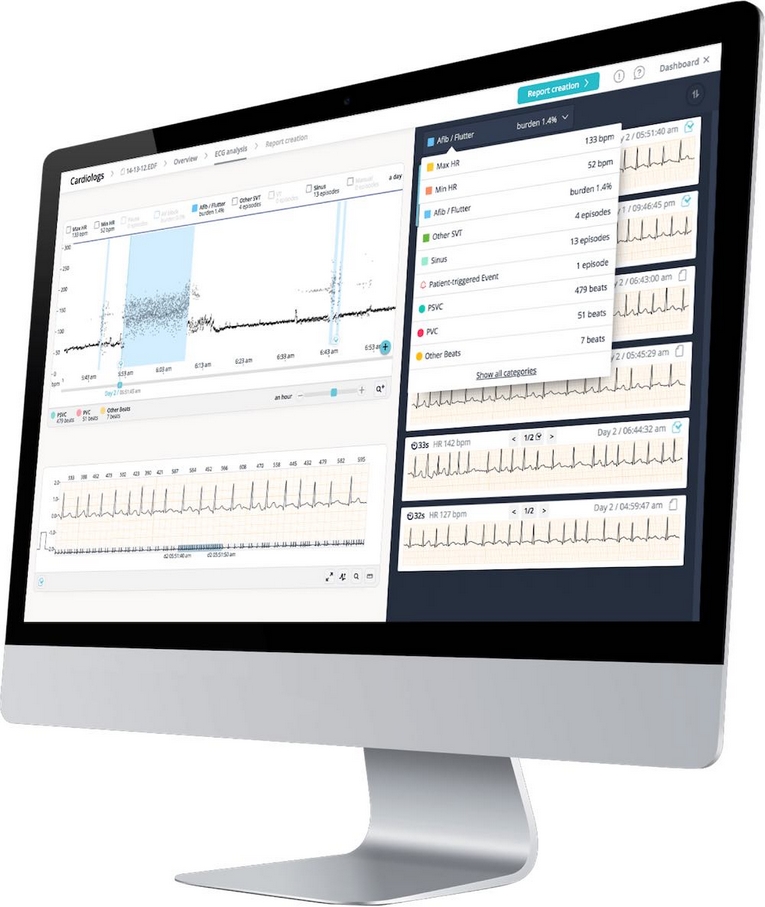
Accélérer l’analyse d’ECG Holter en clinique grâce à l’intelligence artificielle
Publié le 29 octobre 2021

DM connectés : des DM comme les autres au regard de la réglementation ?
Publié le 12 août 2021
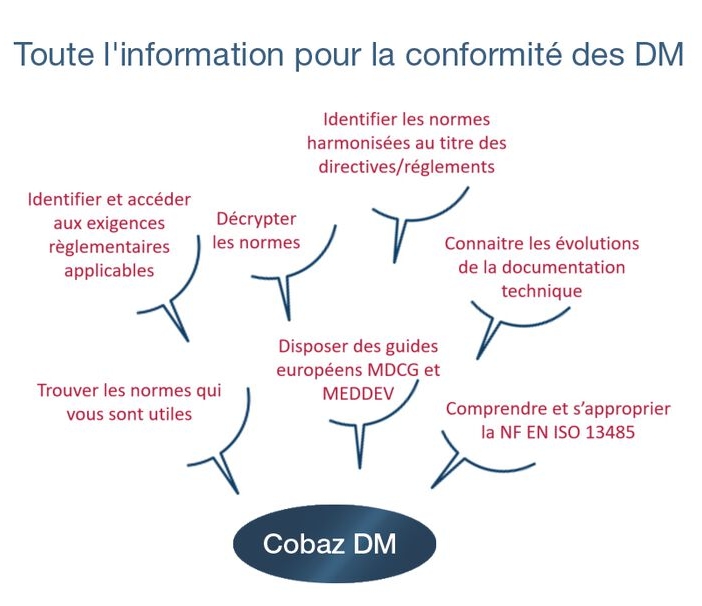
Cobaz DM : un outil dédié pour accéder aux normes et réglementations
Publié le 12 août 2021

Loi Jardé et Règlement (UE) 2017/745 : le point sur la matériovigilance
Publié le 06 juillet 2021
DeviceMed guide de l’acheteur 2021-2022
Publié le 05 juillet 2021
Mon logiciel est-il un dispositif médical en vertu du règlement européen ?
Publié le 21 juin 2021
DeviceMed Mai/Juin 2021
Publié le 06 mai 2021

Test de conformité des dispositifs et emballages médicaux
Publié le 25 mars 2021

DeviceMed Mars/Avril 2021
Publié le 22 mars 2021

AFNOR Certification, 2ème organisme notifié français : à quelle échéance ?
Publié le 02 février 2021

DeviceMed Janvier/Février 2021
Publié le 02 février 2021
IA et DM : un duo gagnant en route sur un parcours semé d’obstacles
Publié le 15 décembre 2020





























